如何迅速看懂一张核磁共振氢谱图?
17 个回答
写在开头,如果你对本文有任何疑问,或者发现任何错误,请及时指出,我会及时做出更改。(别吝啬给个赞再走,我看到好多只收藏不点赞的白嫖,哼!)
另外: 我真的没空解答问题,问的人太多了,而且我有自己的工作,我一天下来挺忙的。
3. 核磁共振 Nuclear Magnetic Resonance (NMR)
核磁共振有包含了 H1-NMR, C13-NMR, DEPT, COSY 等分析技术
我先讲H1-NMR吧,其他的如果需要我再写
(昨晚想了半天,不讲电子自旋没法解题,必须一步一步的来)
3.1. H1-NMR 核磁共振氢谱
化学位移(chemical shift):同种核由于在分子中的化学环境不同而在不同共振磁感应强度下的吸收峰,这称为化学位移。
屏蔽效应和化学位移起因:
分子中磁性核不是完全裸漏的,质子被价电子包围着,这些电子在外界磁场的作用下发生循环的流动,会产生一个感应磁场,感应磁场与外界磁场相反,所以,质子实际上感受到有效的磁感应强度应是外界磁场强度减去磁场强度。
B有效 = B0(1-\sigma)=B0-\sigma B0=B0-B感应
核外电子对核产生的这种作用称为屏蔽效应

影响化学位移的因素
3.1.1.电负性: 电负性大的原子(或者基团)吸电子能力强
吸电子基团降低了氢核周围电子云的密度,屏蔽效应就降低了,质子化学位移向低场移动,左移
同理,给电子基团-----》 氢核周围电子云密度上升 -----》 化学位移向高场
3.1.2. 各向异性效应
当分子中某些基团的电子云排布不成球形对称,它对临近的氢核产生一个各向异性效应的磁场,从而使得某些空间位置接受屏蔽,某些空间位置上去屏蔽(就是没有被屏蔽)
以下,我给出三个例子,来自我的笔记(出处:基础有机化学邢大本)


(看不懂的字请问,怕我字体太难看,有些字你看不懂)
下面我们说耦合常数 coupling constant
想必,你们一定学了这个东西啦,耦合常数定义我就不给你写了,你书上写的比我说的要清楚,然后,你也应该n+1定律,不明白的话我再说一遍好啦
所谓n+1信号,就是一个质子发生的信号会被分裂成两个(n个质子发生的信号会被分裂成n+1个)
但是注意了,如果一个质子被两个质子裂分,的确会看到一个三重峰(被裂分成了2+1个峰),但是这仅仅是这个两个质子(-CH2亚甲基)是在同一个环境中,如果两个质子不是等位氢,那么你就会看到两个双重峰。

所以我们看到三重峰啥意思呢??
有个碳旁边的一个碳,它是CH2
两个二重峰啥意思?
有个碳旁边有两个碳,每个碳上都有个H
四重峰,旁边有 CH3, 双双双重峰,旁边有个三个CH(两个CH是双双重峰,三个就是双双双了,能理解?)
下面我们看题

不用看管其他,我们就看产物三,产物三给出了两组核磁共振氢谱,因为产物三用两种同分异体,化合物1在被硼氢化钠还原羰基的时候,出现了一个立体性选择的问题,所以导致了醇羟基不知道是上面还是下面,那么我们根据这个数值,来分辨以下,表1(左边)和表2(右边)各代表哪个产物。
首先不要管羟基和胺上的H,题中说数据里没有给。
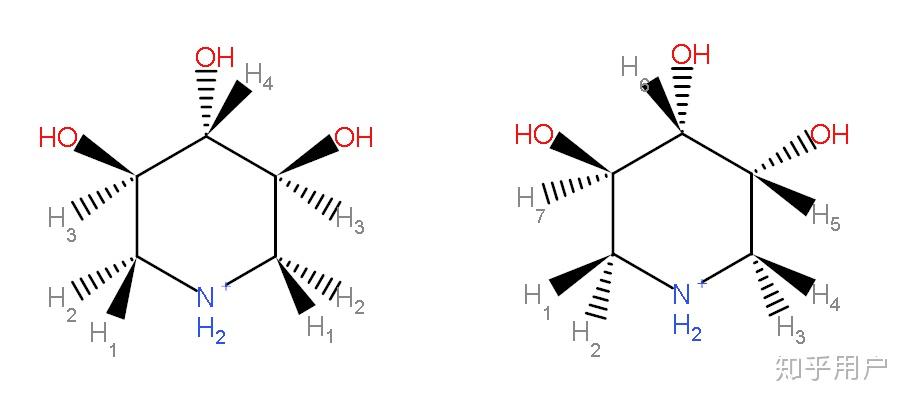
我们看第一个结构式,里面有四个不同位置的氢,已经很好分辨是右表了,同理,第二个就是左表。但是我们一个一个分析每个氢的数据。
第一个结构式
H2 和 H3 不是同一个位置,所以他俩对H1的影响就会是一个双双重峰(double doublet)
所以 H1 ---》 dd (double doublet)
再看 H2 同理,一样被H1和H3裂分成一个双双重峰。
我们再看 H3 被三个不同位置的氢裂分(H1 H2 H4) 所以你会看到 双双双重峰(double double doublet)
H3 ---》ddd
H4? 周围只有H3,两个H3 所以被裂分为(注意是两个H3,相当于CH2,根据n+1)一个三重峰(triplet)
问题来了,我们如何区分H1 和 H2 都是 双双重峰啊
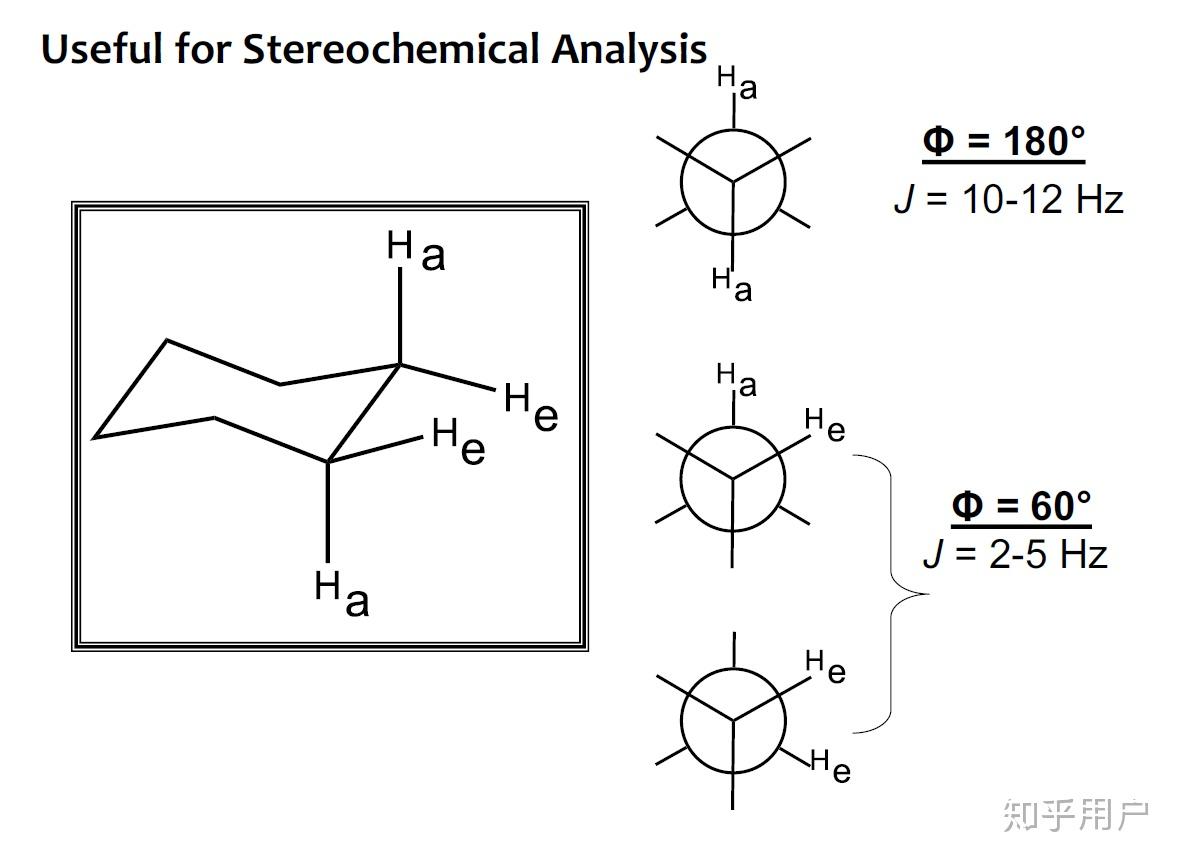
如果两个氢 为180° 则耦合常数在10-12hz,若是 60° 耦合常数在2-5hz

我们画出椅式结构, 我们发现 H2 与 H3 是 60°,H1 和 H3 是 180°
所以根据右表可以知道 J H1-H3 =10.2 Hz, JH2-H3 =4.4 Hz
综上所述
3.72 (2H, ddd, J 10.2, 8.5, 4.4 Hz) 为 H3
3.46 (1H, t, J 8.5 Hz) 为 H4
3.40 (2H, dd, J 12.7, 4.4 Hz) 为 H1
2.86 (2H, dd, J 12.7, 10.2 Hz) 为 H2
对于左表,你喜欢的话,你也可以分析一下。给一个我的分析结果



我们说一个简单的吧,看题

首先 积分比为 1:3:6
对应的分别是 七重峰 单峰 双重峰
算一下不饱和度 ((4*2+2)-10)/2=0
\frac{碳原子数\times 2 +2 - 氢原子数}{2}= 不饱和度
算不饱和度的目的是看这个结构式里有没有双键或者环。
不饱和度=1 含有一个双键,或者环
不饱和度=2 含有两个双键,或者一个三键,或者两个环,或者一个双键和一个环
不饱和度=4 可能含有苯环
这个结构式里面全部都是碳碳单键,因为不饱和度为0
分析峰值 a. 七重峰 根据n+1,说明旁边有六个等位氢把一个氢原子裂分了
很可能是 两个CH3
b. 单峰,说明有一个碳上一个氢都没有(当n=0时,n+1=1 单峰)
c. 双重峰,说明一个氢被另外一个氢裂分,积分为6,说明有六个等位氢被一个氢裂分了。

为什么是醚而不是醇? 从峰的耦合常数我们可以看出来,与电负性基团相连(醚键),向低场位移。
或者。。。。查红外光谱,看官能团的峰位。这时候就体现出红外的作用了。
令群众要求,更新一下C13-NMR 和 COSY 所有内容都是全部手打,更新可能会很慢,也会很长,希望观看之余点个赞,谢啦
3.2 C13-NMR 碳谱
开始的时候先简单介绍下,让我们再回归到最开始的地方,自旋,而且我发现了一个很可怕的东西,我最开始没有讲自旋,那在这里我就慢慢的给大家介绍好了,我也是一个小菜B,化学学的一般,所以我就用我最浅显的语言来讲给大家好啦,以下的内容不会有太多像教科书上的东西,即使有,我也会解释的。看不懂的记得问我,现在我们开始。
我们先说,自旋(spin),学过化学的都知道,大学化学里有很多奇奇怪怪超过人认知的东西,例如成键轨道,反键轨道,这些东西。我们看书,书上说“自旋是粒子的一个内禀性质”。故名思意,自旋就是自己转圈圈,我敢肯定,你脑子里的模型一定是一个地球在自转的样子,正好符合了自旋这个东西,但是事实不是的,你可以这样理解,事实上是粒子会自己产生一个角动量,然后形成‘自旋’这个东西。具体是如何产生的,可能以我的学识,给大家解释清楚特别困难,并且说多了就跑题了。
综上所述,你要接受一个观点就是,一个粒子从‘出生’开始就带有一个内禀性质,这个性质叫做自旋(角动量),就像你出生就可以确定是男生还是女生了,或者是双性人。大概就这个意思。
你接受这个观点以后,我们再继续往下进行,一个自旋为1/2的粒子,会产生一个磁场,而和外部的磁场相互作用就会让你看到核磁共振信号,但是自旋为0的粒子,就不会。例如C12他的自旋为0,没有核磁共振信号,但是C13就会产生核磁共振信号,因为C13的自旋为1/2.
如果以上你没看明白,那么没关系,我们之间进入正题,C13-NMR
(如果你没看明白还想去搞明白,那么建议你去B站搜妈咪说的视频,有一期讲自旋的,讲的特别详细)
C13的化学位移是用四甲基硅烷作为标准的,规定四甲基硅烷的化学位移为0,然而,影响C13的化学位移因素特别多,电子屏蔽和周围电子云的密度都会有影响。
废话不多说,直接上题。
以下例题12道,都是我自己的笔记上来的,我们一边讲,一边学,希望你也可以把这12道题抄下来,仔细搞懂12道题。基本就没什么问题了。
例1

(当然我的答案给出来了。。。我懒得去答案了,我就来解释一下这些来源好了,我今天撑死写几个例子,我还要去学有机,这几天慢慢的给大家写完)
我们看这个例子,一用四个峰,化合物结构式也给你了,要你匹配四个碳分别对应哪四个峰,这个化合物我们很清晰的可以看出,四个碳的化学环境不同,没有等位碳(看不出来的私我)
第一点,先记住(敲黑板,划重点,记笔记)醚,酯,醇类的化合物,化学位移均在50-100
解释:也就是是和醚,酯,醇,这些基团直接相链接的碳,它的化学位移大概在50-100
那么为什么?
解释:碳原子和氧原子相连,氧的电负性大,所以向低场位移(变大)
这样我们就可以如图碳b的位置了吧。
现在问题来了,碳a和碳c距离氧的位置一样啊,我该如何区分ac呢?
第二点,一般情况下!二级碳的化学位移大于一级碳,同理三级碳的化学位移大于二级碳
化学位移 3°>2°>1°
碳a是一级碳,而碳c是二级碳,所以!ac的位置我们可以确定了。
其次d就很好判断了,也因为d离氧最远,所以向低场位移(变小)
看看我们从第一道题里学到了什么?
- 醚醇酯的化学位移
- 碳的级数化学位移
- 和电负性原子越近化学位移越大,反之越远越小
我们继续看题。。。
例2

化合物五个碳,峰有四个,c峰为最大,d为最小,a的高度为其他的二倍。化合物与碳b相连的两个甲基a为等位碳,其他都不存在等位碳。请问谁的化学位移最小?
解释:碳d的化学位移最小,因为碳d为一级碳。
问题又来了,a也是一级碳,为什么a的比d大?
解释:因为,与a相连的是3级碳,而与d相连的却是2级碳

如图,方框里的数字是我标记的相连碳的级数,例如碳a,他和三级碳相连,方框里数字就是3,而碳c他和两个一级一个二级碳相连(2+1+1)数字为4,其他同理
所以,得出结论,如果碳的级数一样,谁链接的碳级数越大,谁的化学位移就高
这也就是为什么a要大于d的原因。
在解释c和d,以上很好判别,三级碳的位移要大于二级碳,我上面说过了,所以不做太多赘述。
例3

看这个题,我圆圈里写的数字就是和与之相连的碳的级数相加,例如碳b,和它相连的有两个一级碳(碳a)和一个二级碳,所以是4(2+1+1)。其他同理。
看图谱,先找最低和最高,圆圈里面的数字最低是2,最高是5。分别对应碳e和碳c,最低和最高就找到了,其次碳a有两个等位碳,所以,最高的峰为是a。现在就是分清碳b和碳d,不用多说,b是4,d是3,所以b要比d大,依次判断。
例4

(翻译)如图是戊烷C-13NMR图谱,显示了三个信号化学位移分别是14,23和34ppm,请匹配这个三个化学位移分别对应哪一个碳。
首先bc都是2级别碳,但是唯独a是一级碳,所以呢。。。a的化学位移最小。比较bc的化学位移还是看和它们相连碳的级数,圆圈里我算出来的分别是3和4,所以b大于c。
例5

一样的分析过程,一样的套路。我们就用这道题来结束一下烷烃的图谱吧。这道题我就不解释了,不懂得问我就好了。
下面我们来说一个新的章节(我真的后悔写这个回答了,真的好长,我真的是在给自己挖坑填)
化学位移和电负性的关系。

如图可见,随着官能团上的原子电负性增加,其与之相连的碳的化学位移越来越大。
(感谢 @求解小白 指出的错误,这里已经做修改)
和电负性强的原子相连的碳,化学位移一定比没用相连的大,或者说靠近。
下面给出几个例子

左上,和氯直接相连的碳就要比没用链接的要大。图示(碳a大于碳c)
右上,最右边的一级碳离氯的距离要比最右边的一级碳近,所以同样两个一级碳最左边的碳化学位移大。(无视一些标注数字,当时笔记有误,看我这里写的就行)
左中,由于溴的电负性不大,所以碳a的化学位移并没有碳b大
左下,碳a和碳b的链接数都是2,但是碘的电负性更小,所以b的化学位移大于a。

上面给出了不同的醇的碳原子化学位移
左边和右边的例子相比较都说明了碳相连的级数越高,化学位移越大。
继续例题
例6

(翻译)如图所示图谱吧啦吧啦。。告诉你了这个物质分子式是C6H14O,通过图谱确定一下结构式吧。
先算不饱和度,IHD(index of hydrogen deficiency)
前面有说过怎么算的,忘了的回去翻。
IHD=(2×6+2-14)/2=0
这说明化合物里面没用不饱和键,如果有的话,双键是1,三键是2,环是1,假设你计算出来IHD是3,可能的结构是1.含有三个双键,2,含有三个环,3,含有一个环两个双键,3,含有一个双键两个环,4,含有一个三键和一个环,5,含有一个三键和一个双键。
既然没有双键,我们首先排除羰基和碳碳双键。
可能的结构就是醇或者醚了,又碳峰比可知,有三个等位碳,其他三个碳并不等位我们可以知道可能存在的结构。因为醇和醚的化学位移都在50-100ppm左右,怎么判断呢,如果是醇的话只可能一个碳在50-100这个范围的化学位移,醚的话,和氧相连接的有两个碳,图中正好符合,在50-100直接有两个峰,所以是醚而不是醇,(醇C-OH,醚C-O-C)能理解吗?
这个时候存在两种同分异构
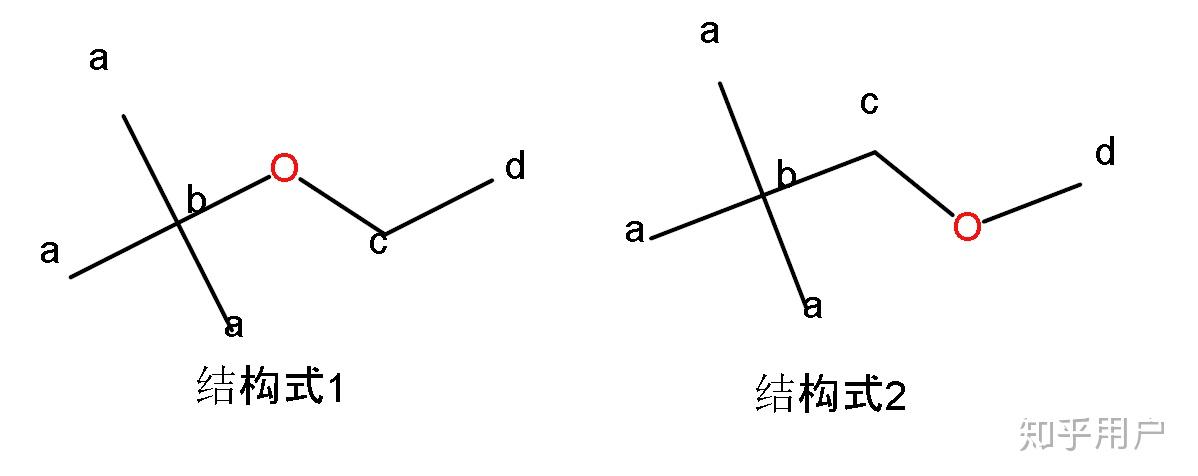
答案是1,但是为什么不是2,如果是结构式2,那么碳c和碳d当之无愧是前面两个峰(50-100ppm)因为他俩和氧相连接,那么最高的那个峰一定是a,可是碳a的链接数是3,碳b的链接数是5,理应碳b的化学位移大于碳a,但是图谱正好相反,所以结构式一完美的契合了。
下面我们来说炔烃

我们在计算炔烃相连的碳级数时,把碳碳三键的碳都当做二级碳。
如图所示,炔烃的化学位移一般在70-100ppm
第一个结构式我就不解释了,第二个结构式我们先计算出它们的相连碳级数,碳c为4所以化学位移要比碳b高,a比e高是因为e距离三键比a远。
第三个结构式,我们可以看出,三键上的碳原子总要高于单键,其次我们再看相连碳级数。
现在看例题
例7

题目说,这个化合物分子式是C6H10但是有两个同分异构体,请正确匹配每个同分异构体对应的结构式。
第一步算IHD
IHD=(2×6+2-10)/10=2
不饱和度为2,可能情况是,两个双键,两个环,或者一个三键。
双键的化学位移在100-150,图中最高没超过80,所以pass,如果是两个环,那么至少三个碳原子才能连城一个环,存在的环数为3元,或者四元,这两者都存在angle strain(我忘了中文叫啥了,不知道的朋友,你自己查一下吧)所以不稳定,其次峰比也对不上。
所以只可能存在一个三键。
题中已经给了提示,左边的是内部炔,右边是末端炔。
先来看第一个,如果是内部炔,存在同分异构体可能为:

只有第一个有六个信号峰,所以是第一个。
第二个五个信号,第三个三个信号。
再看末端炔,因为显示有一个峰比其他峰都高出三倍,说明存在C-(CH3)3
所以

没毛病吧
例8

2-甲基-1-丁烯有五个信号峰,化学位移分别是12,22,31,109,148,请把每一个化学位移对应到每一个碳上。

先计算相邻碳级数,a=3 b=4 c=3 d=4 e=2 (不会算的问我)
109和148肯定是碳ab,由于b的级数大于a,所以b是148,a是109
其次碳级数d>c>e,根据数字依次排列
a为109 b为148 c为22 d为31 e为12
例9

分子式为C8H10,写出化学式。
峰值比为1:2:1
不饱和数算出来 IHD=(2×8+2-10)/2=4
分子式可以一眼看出来绝对含有苯环,题目还限制了三个峰,所以为了保证对称性只可以链接对位,如果是邻位的两个甲基会有四个峰,如果间位会有5个峰值。

a:b:c=2:2:4
苯环上的碳化学位移为128.5左右,碳b相连级数高于碳c所以,c为129,b为135,a为21
写在最后,可能要烂尾了,这个帖子是我大学闲得无聊写的,写起来每个图我还要自己去画,好麻烦,包括整理笔记,再转述出来,不能出错,挺累的,现在也工作了,我看有机会继续发布。
另外不要私信我了,拜托拜托,私信的人好多我压根看不过来
半懂不懂的进,因为你得明白啥是
化学位移(判断大概基团),耦合常数(判断氢键位置),n+1规律(判断峰重数与峰的裂分)
笔记在最下面!(做题用)

步骤:
- 一,计算不饱和度
- 二,排除溶剂峰及其对应水峰
- 三,计算积分曲线
- 四,计算耦合常数
- 五,分析
[例] 某未知化合物M的分子式为C9H8O3,其H-NMR谱(400 MHz,CD3OD)试解析推断其结构

一,计算不饱和度
Ω=(9×2-8+2)/2=6
饱和度>4时大多时候含有苯环
二,排除溶剂峰及其对应水峰

CD3OD氘代甲醇:溶剂峰(3.30)水峰(4.8)


三,计算积分曲线
ABCD峰面积之比为1:2:2:1,推测为
A:1H B:2H C:2H D:1H
如果为ABCD为2442H,则有12H
但是化学式中总氢数为8<12,所以只能是1221H共6个,至于剩下两个,可能是谱图没测出来。
四,计算耦合常数
J=相邻两峰的化学位移之差×仪器磁场强度
- Ja=(7.48856-7.44877)×400=15.9Hz
- Jd=(6.20993-6.16963)×400=15.9Hz
- Jc=(7.34863-7.34372)×400=8.7Hz
- Jb=(6.71477-6.70982)×400=8.7Hz
五,分析
part one
D: δ6.19(1H,d,15.9hz)一个氢邻近有一种化学环境的氢
A: δ7.47(1H,d,15.9hz)一个氢邻近有一种化学环境的氢
解:①化学位移δ6-7 ②J相近 ③一个氢(1H)邻近有一种(双峰d)化学环境的氢CH-CH
①②③→典型双键
又: 邻碳耦合: J(12-18)反式 J(6-12)顺式
所以:反式双键(很典型,记住!)

part two
B: δ6.70(2H,d,8.7hz)两个氢邻近有一种化学环境的氢
C: δ7.34(2H,d,8.7hz)两个氢邻近有一种化学环境的氢CH2-CHn
解:①化学位移δ6-7 ②J相近 ③两个氢(2H)邻近有一种(双峰d)化学环境的氢
①②③→对二取代苯环(很典型,记住!)

知道这里就差不多了,剩下的需要靠红外才能完全推测出相应结构,为

检查答案
现在我们根据它的化学结构再反推谱图试试

- 对称结构(红线标记处为对称轴)→两个H1等价(所以用相同的编号表示),同理,两个H2也等价。
- 两个H1受H2影响,两个H2也受H1影响H3H4同理,所以耦合常数相等

- 而-OH和-COOH的信号没有体现出来所以积分曲线的计算少两个H
笔记:知识补充
一,反推谱图
在这里还想说说能根据化学结构反推谱图更能说明你掌握了,举个例子

除了得明白abc是什么峰还得知道怎么区分:
a和c都是d峰,那在谱图中怎么区分呢?
①a在低场(去屏蔽区 化学位移大)
②a的耦合常数大
二,常见的峰
最典型的峰归纳

基础峰练习(答案在下面)










三,小试牛刀
好,现在根据我举的例子再试一个,看看自己是否已经掌握。

提示:
- 饱和度5,可能有苯环
- bd为溶剂峰水峰
- 积分曲线之比a:c=1:3
- a(2H,s), c(6H,s),对称结构
- a苯环两个对称H,c两个对称-OCH3

知道这么多就差不多了!大家再试试反推谱图看合不合理。
如果以上知识都整明白了,那么一张氢谱图就能看懂个八九不离十了


