NMN(烟酰胺单核苷酸)
详细内容
NMN(烟酰胺单核苷酸)简介
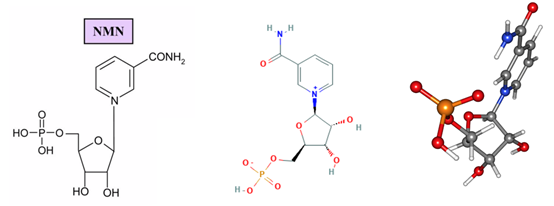
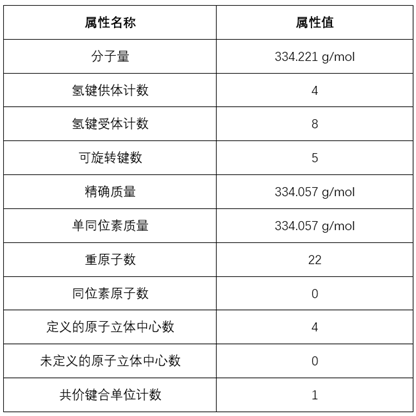
NMN全名nicotinamide mononucleotide,即烟酰胺单核苷酸,是一种自然存在的生物活性核苷酸,NMN有2种不规则存在形式,α和β;β异构体是NMN的活性形式,分子量为334.221 g/mol。

NMN的理化特性
NMN的食物来源
NMN在日常食物中分布较广,蔬菜如花椰菜(0.25–1.12mg NMN/100gm)和大白菜(0.0–0.90 mg NMN/100 gm),水果如鳄梨(0.36–1.60 mg NMN/100 gm)、西红柿(0.26–0.30 mg NMN/100 gm),肉类如生牛肉(0.06–0.42 mg NMN/100 gm)都含有丰富的NMN[1]。

NMN的内源性合成
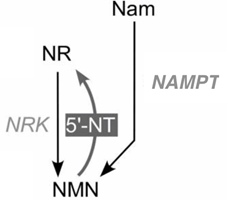
1分子烟酰胺和1分子5-磷酸核糖基-1-焦磷酸(PRPP)在烟酰胺磷酸核糖转移酶(NAMPT或NAMPRT)催化作用下生成1分子NMN和1分子焦磷酸(PPi)。除烟酰胺可生成NMN,1分子烟酰胺核苷(NR)在烟酰胺核苷激酶(NRK)催化下磷酸化生成1分子NMN。
NMN合成酶、消耗酶的组织特异性
(1)NAMPT:NAMPT在体内无所不在,但组织间表达水平存在较大差异。在脑和心脏,NAMPT依赖的补救途径是产NAD+的首选模式;而在骨骼肌,NRK依赖的补救途径是产NAD+的首选模式。
(2)NMNATs(NMN消耗酶):小鼠组织代谢谱表明,NMNAT亚型的活性远高于NAMPT,且除血液外,大多数组织中NMNAT亚型的活性不受限制。
(3)NRKs:NRK亚型的表达分析表明NRK1无所不在,而NRK2主要存在于骨骼肌中。与此一致的是,慢性NR补充引起肌肉的NAD +水平增加,但在大脑或白色脂肪组织收效甚微[2]。
NMN的摄取
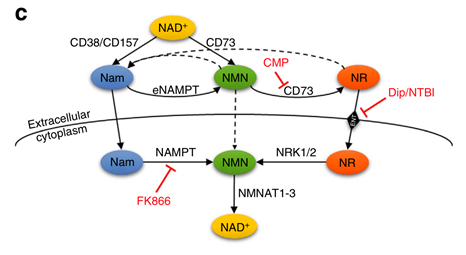
NMN在某些细胞表面有膜转运体,能直接将NMN转入细胞内,所以NMN有两种进入细胞的方式:
①通过转运体直接进入细胞:在2019年初,nature metabolism一篇论文证实了该想法,文章发现小鼠小肠内有NMN特异性转运体存在,叫做Slc12a8,这是一种氨基酸和多胺转运体,对NMN有很高的选择性,并不转运和NMN结构甚为相似NaMN[3]。
②通过细胞膜表面的CD73去磷酸化为NR(通过平衡核苷转运蛋白ENTs)进入细胞内,随后再通过细胞质的NRK酶催化为NMN,进入线粒体被利用(线粒体无NRK)[4]。
NAM既是NMN的前体,又是NAD+经NADase活性消耗途径CD38水解后的产物。因此NAD+的合成、利用、再生是一个涉及胞内胞外的NMN/NR→NAD+→NAM→NMN的循环。
口服NMN对NAD+的促进
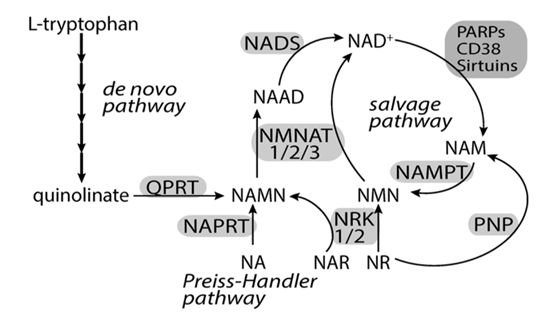
NMN是NAD+的前体,其功能也主要通过NAD+(烟酰胺腺嘌呤双核苷酸)体现。
在补救合成途径中,烟酰胺核糖(NR)或烟酰胺(NAM)经NRK(烟酰胺核苷激酶)或NAMPT、NMNAT合成烟酰胺单核苷酸(NMN),NMN经NMNAT1-3酶合成NAD+。
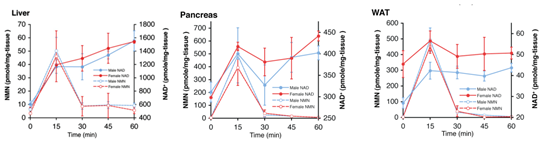
虽然不能在血清中检测到完整结构的NMN,口服NMN仍能够很快(15min)提高雌性、雄性小鼠的NAD+水平[5]:
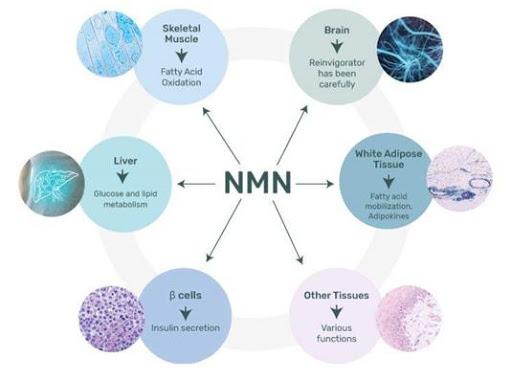
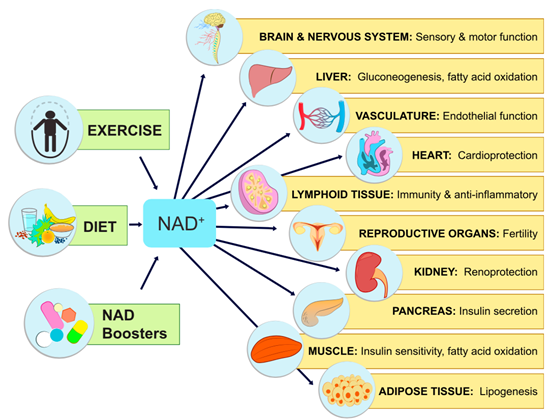
NMN的作用
NMN主要通过转化为NAD+发挥作用,NAD+又名辅酶I,全称烟酰胺腺嘌呤双核苷酸,它广泛分布在人体的所有细胞内,参与上千种生物催化反应,是人体内必不可少的辅酶。
衰老过程中NAD+的下降被认为是导致疾病和残疾的主要原因,如听力和视力丧失,认知和运动功能障碍,免疫缺陷,自身免疫炎症反应失调导致的关节炎、代谢障碍和心血管疾病。
因此,补充NMN提高了体内NAD+含量,从而延缓、改善、防止衰老相关的多种表型,或年龄诱导的代谢紊乱与老年疾病。
A、NAD+与昼夜节律
NAD+依赖的脱乙酰酶SIRT1通过连接调节NAD+补救途径的酶反馈回路和昼夜节律转录-翻译反馈回路,成为昼夜节律与代谢之间的桥梁。
NAD+调节生物钟是通过SIRT1实现的。SIRT1将BMAL1和PER2去乙酰化,而这和CLOCK的乙酰化功能是拮抗的,所以SIRT1能抑制CLOCK- BMAL1介导的clock genes的转录。因此,NAD+通过自身水平影响SIRT1去乙酰化活性,从而反过来影响包括NAMPT在内的一系列生物钟相关蛋白的表达[6]。
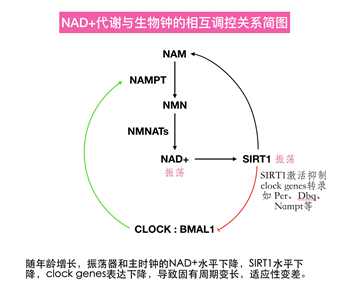
生物钟调节和很多疾病相关,包括但不限于睡眠障碍、糖尿病、肿瘤。很多病理过程都被生物钟紊乱触发,这种紊乱可能来自于遗传,也可能来源于环境,总而言之,保持生物钟正常工作在维持健康方面有重要作用。
B、NAD+与神经系统
Sirtuins是一种依赖烟酰胺腺嘌呤二核苷酸(NAD+)的脱酰基酶,传统上认为它与哺乳动物的热量限制和衰老有关。这些蛋白在衰老过程中对维持神经元的健康也起着重要作用。
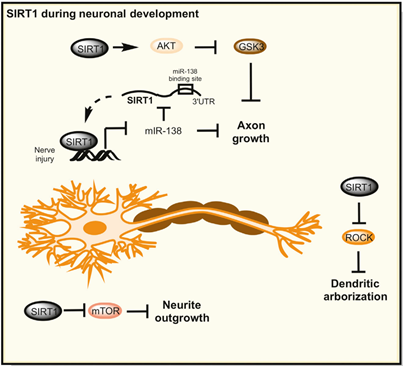
在神经发育过程中, SIRT1在结构上起着重要作用,通过Akt-GSK3通路促进轴索生长、神经突生长和树枝状分支。突触的发育和突触强度的调节对记忆的形成至关重要,而sirtuins蛋白不论在生理还是损伤后,都对这一过程中起重要调节作用。SIRT1在海马体可以以抑制型复合体形式存在,该复合体包含能调控microRNA-134的转录因子YY1。microRNA-134的分布具有脑特异性,能调控cAMP反应结合蛋白(CREB)和脑源性神经营养因子(BDNF)的表达。这对于突触的形成和长期的增强都很重要[7]。
在神经疾病发生发展中,SIRT1在阿尔茨海默氏病、帕金森氏病和运动神经元病等多种神经退行性疾病中发挥保护作用[8],这些疾病可能与SIRT1在代谢、抗应激和基因组稳定性方面的功能有关。激活SIRT1的药物可能为治疗这些疾病提供一种有希望的方法。
C、NAD+与癌症
增加NAD+水平治疗癌症的研究显示:①NMNAT3过表达提高了线粒体NAD+水平,抑制胶质母细胞瘤细胞的生长;②补充NA或NAM能抑制SCID小鼠的肿瘤生长和多器官肿瘤转移。
其原理有:过量的NAD+会促进线粒体呼吸,降低糖酵解,抵消癌细胞喜欢的Warburg代谢(比起氧化磷酸化更依赖于糖酵解的癌细胞能量代谢特性);增加NAD+也会增加SIRT1和SIRT6的活性,两者都通过下调β-catenin信号、下调糖酵解抑制肿瘤[9]。
不过这当中也存在矛盾与担忧:NAD+促进DNA修复和血管生成,有可能帮助癌细胞生长(既有的对野生型小鼠的长期研究未能提供促使肿瘤增加的任何证据)[10]。而降低肿瘤NAD+水平后,随着PARPs修复DNA损伤的能力降低,癌细胞/组织对化疗药物的敏感性将增加。在标准癌症模型中进一步测试NAD+补充剂的效果将非常重要。
D、NAD+与肝功能
已知NAD+信号通路中的酶可以保护肝脏不受脂肪堆积、纤维化和胰岛素抵抗的影响,这些都与脂肪肝疾病的发生有关。
NAMPT在高脂膳食诱导脂肪肝发生发展的过程中起关键调节作用:抑制NAMPT将使高脂膳食造成的肝脂肪变性更严重,过表达NAMPT显著改善肝脂质积累;这种调节作用是通过“抑制NAMPT→减少NAD+→抑制SIRT1→减弱SREBP1的去乙酰化→SREBP1活性降低→FASN和ACC表达上调”产生的。
SIRT1及其下游靶点PGC-1a、PSK9和SREBP1维持线粒体功能、胆固醇转运和脂肪酸稳态。SIRT2通过去乙酰化磷酸烯醇丙酮酸羧激酶来控制糖异生;SIRT3调控OXPHOS、脂肪酸氧化、酮生成和抗氧化应激;SIRT6控制糖异生[11]。
由于这些通路在肝脏中的重要性,维持NAD+水平对于维持器官良好功能必不可少。正常情况下,由于肥胖和衰老,NAMPT水平下降,CD38水平升高,导致到中年时,稳态NAD+水平下降2倍。
将NAD+水平提高到年轻水平在预防和治疗肥胖、酒精性脂肪性肝炎和NASH方面收效显著,同时还能改善葡萄糖稳态和线粒体功能障碍,改善肝脏的健康,增强其再生能力,保护肝脏免受肝毒性损害。
E、NAD+与肾功能
老年肾脏中NAD+水平的降低和sirtuin活性的相应降低在很大程度上是肾功能和顺应性随年龄下降的原因。
①通过NAD+补充激活SIRT1和SIRT3保护高糖诱导的肾系膜细胞肥大,而用NMN治疗小鼠以SIRT1依赖性的方式保护顺铂诱导的急性肾损伤(AKI)[12]。
②5-氨基咪唑-4-羧胺核苷可刺激AMPK活性,增加NAD+水平,并以sirt3依赖的方式保护顺铂诱导的AKI。
③小鼠补充NAM可刺激肾脏保护前列腺素PGE2的分泌,提升缺血后肾功能;NAM也可通过刺激NAD+合成抑制顺铂诱导的AKI 。
F、NAD+与骨骼肌
与年轻的野生型小鼠相比,小鼠的肌肉萎缩和炎症标志物以及胰岛素信号和胰岛素刺激葡萄糖摄取能力下降。用NAD+前体治疗老年小鼠可显著改善肌肉功能。
用NMN (500 mg/kg/day ip .连续7天)治疗老年小鼠,可以通过增加线粒体功能、增加ATP生成、减少炎症、将糖酵解II型肌肉转变为氧化纤维型肌肉,逆转与年龄相关的有害变化。
G、NAD+与心脏功能
NAD+水平对正常心脏功能和损伤后的恢复至关重要。在所有NAD+依赖的信号蛋白中,SIRT3似乎是最重要的:
①SIRT3敲除小鼠的OXPHOS酶高度乙酰化,ATP减少,对主动脉收缩高度敏感,可能是由于线粒体通透性过渡孔的调节因子CypD的激活。
②SIRT3-KO鼠在13个月大时就会出现纤维化和心肌肥厚,随着年龄增长,病情进一步加剧,而NMN治疗可以逆转这种下降。
③无论是缺血前30分钟(500 mg/kg, i.p.)或再灌注前和再灌注期间的重复给药,使用NAMPT过表达或NMN治疗都能显著防止压力过载和缺血-再灌注损伤,使梗死面积减少44%左右。
④使用NAD +前体治疗也提高了老年MDX心肌病小鼠的心脏功能。
⑤NAD+前体改善了缺铁诱导的心力衰竭小鼠模型的线粒体、心脏功能。
⑥NAD+前体甚至可以通过激活SIRT3保护并恢复弗里德希氏共济失调(FRDA)心肌病小鼠模型的心脏功能到基本正常水平。
H、NAD+与血管内皮细胞
内皮细胞(EC)衰老是一个结构和功能改变的病理生理过程,包括血管张力失调、内皮通透性增加、动脉硬化、血管生成和血管修复受损、EC线粒体生物生成减少等。
细胞周期失调、氧化应激、钙信号改变、高尿酸血症和血管炎症与EC衰老和血管疾病的发生、发展密切相关。许多异常的分子通路与这些潜在的病理生理变化有关,包括SIRT1、Klotho、成纤维细胞生长因子-21和肾素血管紧张素-醛固酮系统的激活。
因为SIRTs和血管衰老的关系,NAD+前体NMN的补充并且已经在一些研究中体现出效果:
①NMN治疗老年小鼠(8周内每天给药300 mg/kg)可恢复颈动脉内皮依赖性扩张(内皮功能的一种测量方法),同时降低主动脉脉搏波速和弹性动脉刚度。
②NMN (500 mg/kg/天,水送服,持续8天)对小鼠的治疗取得显著疗效:通过促进sirt1-依赖的毛细血管密度的增加,改善了老年小鼠的血液流动和耐力。
③NMN通过改善老年小鼠年龄诱导的血管内皮功能障碍以及神经血管耦合(NVC)反应,显著提高老年小鼠认知,并且NMN降低老龄鼠脑微血管内皮细胞的线粒体ROS,恢复NAD+、线粒体能量。
在血管内皮中增加NAD+水平将可能成为一种增加老年人的活动能力潜在疗法,并能治疗因血流减少而发生发展的疾病如:缺血-再灌注损伤、伤口愈合缓慢、肝功能障碍和肌肉肌病等。
I、NAD+与代谢障碍
NMN对脂肪代谢、糖代谢紊乱导致的肥胖、Ⅱ型糖尿病、生殖抑制都有改善作用,甚至能够改善肥胖母亲对雌性后代生殖的不良影响。

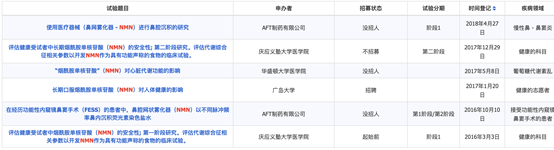
NMN临床实验
目前登记在案的NMN长期临床试验有4起,在Clinicaltrials. Gov等网站可以查询,但相关数据均未被披露: