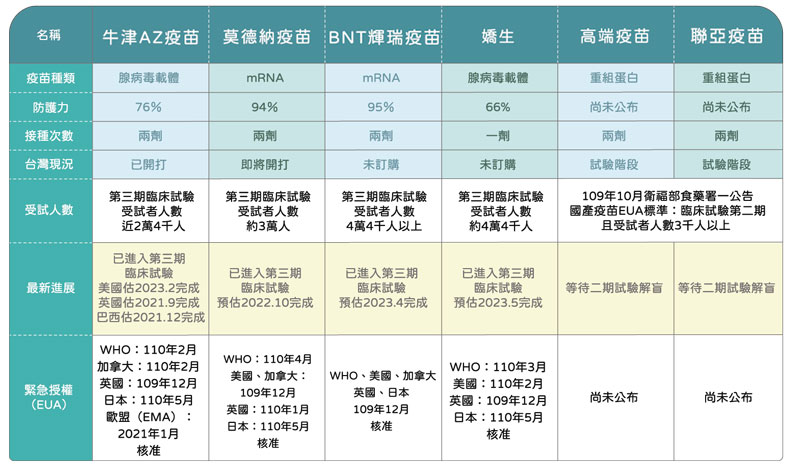
台灣對於疫苗採購一事爭論不休。但除了關注台灣何時有足夠疫苗之外,民眾更好奇的是,AZ、莫德納、BNT、嬌生、高端、聯亞等,六支由不同廠牌所研發的新冠疫苗,在保護力、施打方式上,有什麼差異呢?《健康遠見》整理新知、讓您一圖看懂。
隨著國內新冠本土疫情升溫,取得疫苗自然也成為台灣防疫的迫切課題。世界衛生組織(WHO)歐洲區域辦事處主任也於日前警告,在至少70%人口接種疫苗後, COVID-19疫情才會結束。
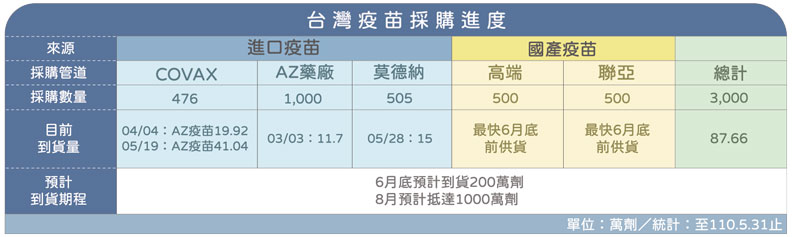
截至5月底,台灣僅取得87.66萬劑進口疫苗
而根據指揮中心日前公布資料指出,若以涵蓋我國人口之65%為規劃,預計為1,500萬人接種,以每人2劑估算,至少需3,000萬劑疫苗。
雖然,指揮中心於日前表示,已完成採購COVAX、AstraZenca及Moderna疫苗約2,000萬劑。並於5月28日與高端疫苗生物製劑有限公司及聯亞生技開發股份有限公司簽訂「國內COVID-19疫苗採購契約」,採購兩家各500萬劑疫苗。
但事實上,截至110年5月31日為止,實際抵台,也就是衛福部真正拿到手、可供國人施打的,僅有87.66萬劑的進口疫苗。
企業、民間團體發聲:願助政府對外洽購新冠疫苗
面對台灣疫苗數量短缺的情況,台灣各企業及民間團體,包括由郭台銘創辦的永齡基金會、佛光山所屬的國際佛光會、慈濟等單位,也紛紛主動表示,願意協助政府對外向原廠國外採購,甚至捐贈BNT、嬌生等進口新冠疫苗。
就連日本外相茂木敏充也於5月28日證實,日本政府正在研擬討論提供台灣部分AZ疫苗等相關事宜。隨著這些消息的傳出,也讓國人不免引頸期待,希冀上述流程能夠快速走完,讓台灣能先取得一定數量的疫苗,供第一線醫護、防疫人員及民眾施打,防止疫情持續擴散。
六大新冠疫苗保護力差異?一張圖表帶您輕鬆看懂!
除了關注台灣何時才能有足夠的疫苗數量供全民施打外。對於一般民眾來說,另一關心的重點自然就是,AZ、莫德納、BNT、嬌生、高端、聯亞等六支不同的廠牌的新冠疫苗,在保護力、施打方式上,有什麼差異呢?一起來看看《健康遠見》為您整理的相關資料。
牛津AZ疫苗(AstraZeneca)
名稱:AZ疫苗又稱牛津疫苗,是由阿斯特捷利康(AstraZeneca)藥廠與英國牛津大學與合作研發的新冠疫苗。
製作方式:屬於「腺病毒載體」疫苗的一種,是透過改良的黑猩猩的腺病毒(ChAdOx1)當載體而製成的疫苗。
保護力:根據阿斯特捷利康公司公佈資料,AZ疫苗保護力約76%左右。至少要接種兩劑,兩劑建議間隔8~12週,才能發揮完整保護力。
臨床試驗:AZ 疫苗的臨床試驗於多國進行,包括在英國、巴西、南非進行第一至三期臨床試驗。該研究於2020年4月23日至11月4日間進行,共有近2萬4千名之受試者。目前已進入第三期臨床試驗階段,預估美國於2023年2月、英國在2021年9月、巴西2021年12月完成。
緊急授權:WHO、加拿大於110年2月,英國在109年12月,日本於110年5月,而歐盟(EMA)則2021年1月核准。美國FDA迄未核准AZ疫苗的緊急使用授權。
副作用:除了注射部位腫痛、發燒、疲倦、肌肉痠痛外。國外也傳出不少罕見血栓、腦靜脈栓塞個案。
歐盟藥品管理局(EMA)安全委員會曾於2021年4月發表聲明表示:「不尋常的血栓與低血小板應該列為AZ疫苗的非常罕見副作用。」但EMA和世界衛生組織(WHO)皆建議繼續施打AZ疫苗,原因是考量染疫風險,利仍大於弊。
莫德納疫苗(Moderna)
名稱:Moderna COVID-19疫苗,又名mRNA-1273疫苗,由美國生物技術公司開發。
製作方式:屬於mRNA疫苗的一種。
保護力:第三期臨床試驗於美國進行,研究期間為2020年7月27至 10月23 日,共納入了3萬餘名受試者。試驗結果發現,在第一劑、第二劑間隔28天,接種兩劑下,保護力可達94.5%。
且疫苗效力亦未因年齡、性別、種族不同而有明顯差異。第三期臨床試驗預估最終於2022.10完成。
緊急授權:WHO於110年4月,美國、加拿大於109年12月,英國在110年1月,日本於110年5月核准。
副作用:以注射部位疼痛、倦怠、頭痛、肌肉痛、發燒…為主,一般而言症狀輕微、數天後即可緩解,接種第二劑後出現反應的比率較第一劑為高。約 1%受試者出現「嚴重」不良事件,但發生頻率在疫苗組和對照組並無不同。
其他關注到的特殊事件包括局部淋巴結腫、顏面神經麻痺、及過敏反應,但皆未顯示有疫苗安全上的疑慮,另在試驗中並未有嚴重過敏性反應(anaphylaxis)發生。
BNT輝瑞疫苗(Pfizer-BioNTech)
名稱:輝瑞疫苗名稱為BNT162b2。是由美國藥廠(Pfizer)與德國生技公司(BioNTech)共同研發,又可稱為BNT疫苗。
製作方式:屬於mRNA疫苗的一種。
保護力:BNT疫苗目前適用接種年齡為16歲以上,採肌肉注射,接種劑次為兩劑量,兩劑需間隔 21天以上。
其第二/三期臨床試驗於包括美國、阿根廷、巴西、南非、德國、土耳其等多國進行。研究期間為2020年7月27日至11月14日,共納入逾4萬名受試者。
研究結果顯示,接種完第二劑疫苗後七天,保護力為95%,且疫苗效力亦未因年齡、性別、種族不同而有明顯差異。第三期臨床試驗預估最終於2023年4月完成。
緊急授權:WHO、美國、加拿大、英國、日本等國皆於109年12月核准。
副作用:臨床試驗結果指出,BNT疫苗常見接種後反應為注射部位疼痛、疲倦、頭痛為主。試驗中觀察到的不良事件包括局部淋巴結腫、顏面神經麻痺,以疫苗組發生的比例較高。
而嚴重的不良事件(serious adverse events),疫苗組、對照組的發生率都不高,且並無差異,未顯示有疫苗安全上的疑慮。
嬌生(Johnson&Johnson)
名稱:嬌生疫苗又可稱為Ad26.COV2.S疫苗,由嬌生旗下楊森藥廠(Janssen Pharmaceuticals)與美國醫療中心,共同合作開發。
製作方式:屬於「腺病毒載體」疫苗的一種,是透過改良的黑猩猩的腺病毒(ChAdOx1)當載體而製成的疫苗。
保護力:目前可施打於18歲以上成年人,施打一劑能達到66%的保護力,第三期臨床試驗受試者人數約4萬4千人,預估最終於2023年5月完成所有第三期臨床試驗。
緊急授權:WHO於110年3月,美國於110年2月,英國於109年12月,日本在110年5月分別核准。
副作用:美國傳出極少數血栓案例,歐盟藥品管理局(EMA)曾表示,血栓應列為AZ和嬌生疫苗的罕見副作用;但EMA和世界衛生組織(WHO)皆建議繼續施打這兩支疫苗,原因是考量染疫風險,利仍大於弊。
高端疫苗
製作方式:為重組蛋白疫苗。
保護力:尚未公布,等待二期試驗解盲中,預計6月中旬左右公布。根據指揮中心5月31日公布資料,高端疫苗第一劑試驗人數為3852人(老年人846位);第二劑試驗人數為3815人(老年人838位)。
緊急授權:尚未公布。根據109年10月衛福部食藥署公告國產疫苗EUA標準:至少需進行第二期臨床試驗,且受試者人數達3000人以上。
副作用:未知。
聯亞疫苗
製作方式:為重組蛋白疫苗。
保護力:尚未公布,等待二期試驗解盲中。根據指揮中心5月31日公布資料,聯亞疫苗第一劑試驗人數為3875人(老年人799位);第二劑試驗人數為3844人(老年人792位)。
緊急授權:尚未公布。根據109年10月衛福部食藥署公告國產疫苗EUA標準:至少需進行第二期臨床試驗,且受試者人數達3000人以上。
副作用:未知。