數位時代
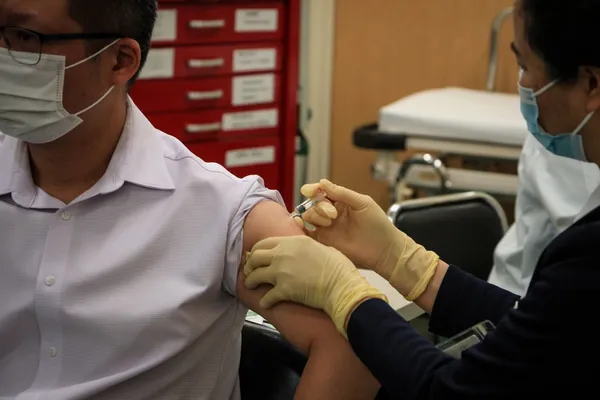
台灣新冠肺炎疫苗從哪來?誰先施打?指揮中心:3 種人不可接種 AZ 疫苗
新冠狀病毒(COVID-19,俗稱武漢肺炎)疫苗是近日大家最關心的事情,《數位時代》整理疫苗的最新進展,持續為讀者更新。
台灣的疫苗從哪來?何時到貨?
中央流行疫情指揮中心指出,台灣將以 3 種形式:「國際投資」(世界衛生組織主導,疫苗取得機制 COVAX)、「逕洽廠商購買」及「國內自製」方案取得新冠疫苗。
指揮官陳時中 2 月 21 日表示,台灣目前確定到手的疫苗有 1981 萬劑,未來最少會有 3000 萬 劑,疫苗最大值會到 4500 萬劑,其中國產疫苗將占 2000 萬劑,由國內 2 家疫苗業者各提供 1 千萬劑。
其中預計最快取得的是約 20 萬劑的阿斯特捷利康(AstraZeneca, AZ)疫苗。食藥署署長吳秀梅 2 月 20 日表示已核准 AZ 疫苗的緊急使用授權,若疫苗廠資料完整,預計最快抵台 7 天後可接種。
而與美國莫德納(Moderna)公司簽署的 505 萬劑疫苗,預計將於第 2 季開始供貨。該疫苗係為多劑型包裝(每瓶 10 人份),存放於 -20℃ 可保存 6 個月,於 2-8℃ 之使用期限為 30 天,依臨床試驗結果,每人需施打 2 劑,2 劑間隔 28 天,疫苗保護效力可達 94%。
| 疫苗來源 | 劑量 | 提供時間 |
|---|---|---|
| 英國牛津大學與阿斯特捷利康(AZ) | 1000 萬劑 | 未定 |
| 莫德納 | 508 萬劑 | 預計今年第 2 季提供 |
| COVAX 機制 | 456 萬劑 | 預計 3 月抵台 20 萬劑 |
| 美國輝瑞與德國 BioNtech(BNT) | 500 萬劑 | 溝通中 |
| 國內廠商 | 共 1000 萬劑 | 二期臨床試驗中 |
誰能先打疫苗?去哪裡施打?
依職業、年齡、重大疾病排序。根據指揮中心「COVID-19 疫苗接種對象優先順序」,共有 9 大順序、1358 萬人將優先接種疫苗。
AZ 疫苗施打建議 3 類人不能接種
台灣已有首批 AZ 武漢肺炎(2019 冠狀病毒疾病,COVID-19)疫苗,中央流行疫情指揮中心亦公布 AZ 疫苗施打建議。建議不可施打疫苗者包含:
- 對疫苗所含成分過敏者
- 施打第一劑 AZ 疫苗後出現急性嚴重過敏反應者
- 18 歲以下青少年
另有急性嚴重疾病且伴隨發燒或急性感染者,應暫緩施打AZ疫苗。
有以下狀況者,則應謹慎評估施打疫苗的效益及風險,再決定是否施打 AZ 疫苗。包含:
- 血小板減少或任何凝血功能異常(如血友病)
- 免疫功能不全者(包括接受免疫抑制劑治療)
- 懷孕或是可能懷孕的女性
- 正在哺乳的女性
台灣國產疫苗研發現況
聯亞生技
疫苗原理: UB-612 疫苗針對 SARS-CoV-2 病毒高精準設計(high precision design),為全球首創之 COVID-19 多重表位次單位疫苗(Multitope Protein/Peptide-based Vaccine, MPV)。
最新進展: 今年 1 月底獲得食藥署核准第二期臨床試驗執行,希望於一個月內完成約 3,000 位受試者收案並施打第一劑,目標 6 月中提交二期臨床試驗報告向食藥署提出緊急使用授權(EUA)申請,於 7 月開始供應疫苗。
公司產品與專案: 豬口蹄疫合成肽疫苗、公豬去勢合成肽疫苗、豬環狀病毒疫苗 、豬藍耳病疫苗 、阿茲海默症治療性疫苗、愛滋病治療性疫苗
高端疫苗
疫苗原理: MVC-COV1901 新冠肺炎疫苗開發案,抗原設計技轉自美國國衛院(NIH),建構以三聚體結構呈現的 S-2P 全長基因修飾重組棘蛋白作為疫苗抗原,並採用美國 Dynavax 之 CpG1018 佐劑,由高端疫苗公司完成早期開發,篩選出候選疫苗免疫組合物。
最新進展: MVC-COV1901 於 2020 年底獲台灣衛福部人體二期臨床試驗許可,並已順利展開受試者施打。
第二期臨床試驗將採取雙盲、隨機、多中心試驗設計,招募 3,700 名 20 歲以上之受試者,以進一步進行大規模之疫苗安全性與免疫生成性評估。國內將有北中南共計 11 個醫院進行收案,分別為:臺大醫院、林口長庚、北醫附設醫院,三軍總醫院、台北榮總、中國醫藥大學附設醫院、台北萬芳醫院、行政院衛生署桃園醫院、彰化基督教醫院、成功大學醫學院附設醫院、和高雄醫學大學附設中和紀念醫院。
公司產品與專案: 登革熱疫苗、新型流感模擬疫苗、腸病毒 71 型疫苗、Anti-RSV 生物相似藥。
國光生技
疫苗原理: AdimrSC-2f vaccine (COVID-19 S 蛋白片段)候選疫苗,採重組蛋白技術。
最新進展: 1 月 27 日,國光生技宣布將先在海外執行二期臨床,且因應新冠病毒出現變異病毒株,國光生技已開始追蹤病毒株突變情況,開發新一代次世代疫苗。
國光生技去年 8 月進行新冠疫苗第一期臨床試驗,是第一家獲得食藥署准許的國內公司,但去年 12 月因劑量問題無法進入二期臨床試驗。
公司產品與專案: 三價流感疫苗、四價流感疫苗、H1N1 新型流感疫苗、日本腦炎疫苗、破傷風類毒素、結核菌淨素。
(本文轉自數位時代)



