ジョン・ドルトン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/03/31 07:15 UTC 版)

| ジョン・ドルトン | |
|---|---|
 | |
| 生誕 |
1766年9月6日 グレートブリテン王国 グレートブリテン王国  イングランド カンバーランド州 イーグルスフィールド イングランド カンバーランド州 イーグルスフィールド |
| 死没 |
1844年7月27日(77歳) グレートブリテン及びアイルランド連合王国 グレートブリテン及びアイルランド連合王国  イングランド マンチェスター イングランド マンチェスター |
| 主な指導学生 | ジェームズ・プレスコット・ジュール |
| 主な業績 |
原子説 倍数比例の法則 ドルトンの法則 |
| 署名 | |
| プロジェクト:人物伝 | |
生い立ち
カンバーランド州イーグルスフィールドで、クェーカー教徒の一家に生まれる。機織りの息子であり、地元の小学校で初等教育を受けたが、そこの教師が1778年に引退すると12歳にして教師となった。15歳のとき兄と共に近くのケンダルでクェーカー教徒の学校を運営。1790年ごろ法律家か医師になることを志したが、当時のイングランドでは非国教徒は大学に入学できなかったため親族に反対され、1793年までケンダルに留まり、その後マンチェスターに引っ越した。盲目の哲学者で博物学者のジョン・ゴフ (en) に師事して科学知識を身につけ、新たに創設されたマンチェスター・アカデミー(後のハリス・マンチェスター・カレッジ)で数学と自然哲学の教師になった。1800年までそこで教師を続けたが、大学の財政が悪化したため職を辞し、数学と自然哲学の家庭教師として働くことにした。
若いころのドルトンはイーグルスフィールドのクェーカー教徒エリヒュー・ロビンソンに強く影響を受けている。ロビンソンは有能な気象学者で機器製作者であり、ドルトンに数学と気象学への興味を植えつけた。ケンダルにいたころ、ドルトンは Gentlemen's and Ladies' Diaries 紙に寄せられた様々な問題や疑問に答えており、1787年から気象学に関する日記をつけ始めた。その後の57年間で日記には20万以上の気象観測記録が記された[1]。同じころジョージ・ハドレーの大気循環理論(ハドレー循環)を独自に再発見している[2]。ドルトンの最初の出版物は Meteorological Observations and Essays (1793) で、後の発見の萌芽がいくつか見られる。しかしその独創的論文に他の学者が注目することはほとんどなかった。2作目の Elements of English Grammar は1801年に出版。
色覚異常
1794年、マンチェスターに移って間もなく、ドルトンは Manchester Literary and Philosophical Society、通称 "Lit & Phil" の会員に選ばれた。その数週間後自らの色覚を題材にした論文を発表し、先天色覚異常が眼球の液体培地の変色によって起きるという仮説を提唱した。西欧近代科学においては、ドルトンが自らの色覚を観察し発表するまで先天色覚異常に関する学術研究が行われていなかったとの定説がある。ドルトンの仮説の誤りは存命中に明らかになったが、研究の先駆性が評価され、先天色覚異常をドルトニズムと呼ぶようになった。ドルトンの死後保存された眼球の組織を1995年に調査したところ、ドルトンの先天色覚異常は中波長の錐体細胞(M-錐体)が働かないもの(2型2色覚)であることが判明した。なお、ドルトンは論文で次のように記している。
この論文に続いて、雨と露、湧水の起源、熱、空の色、水蒸気、英語の助動詞と分詞、光の反射と屈折といった様々な主題の論文を書いた。
原子説
1800年、Manchester Literary and Philosophical Society の職員となり、翌年には "Experimental Essays" と題した一連の重要な論文を発表。気体の混合物について、真空または大気中での様々な温度における水蒸気や他の蒸気の圧力について、蒸発について、気体の熱膨張率について論じた。この4つの論文は1802年の Lit & Phil の学会誌 ' 2番目の論文は次のような強烈な意見表明から始まる。
純粋な気体を冷却し高圧をかけることで影響を与えることを諦めるべきではない。
0℃から100℃までの様々な温度での水蒸気圧の測定実験の後、ドルトンは6種類の異なる液体の蒸気圧を観察し、同じ温度変化による蒸気圧の変化は液体の種類に依存しないと断定した。
4つめの論文では次のように記している。
空気が温度に比例して膨張することから、定圧状態のあらゆる弾性流体は水銀柱のように加熱によって等しく膨張すると結論付けられない十分な理由はない。したがって、他の物質よりも弾性流体について絶対量と熱の性質から一般法則が導き出しやすいと思われる。
ドルトンの法則
つまりドルトンは、ジョセフ・ルイ・ゲイ=リュサックが1802年に発表したゲイ=リュサックの法則またはシャルルの法則に到達していた。その後2、3年間、ドルトンは同様のテーマの論文を発表し、1803年の水や他の液体による気体の吸収についての論文でドルトンの法則と呼ばれるようになる分圧の法則を提示した。
ドルトンの研究の中でも最も重要とされているのは、化学的原子説である。彼が原子説に到達したのは、エチレンとメタンの研究または亜酸化窒素と二酸化窒素の分析が元になったという説があるが、どちらもトマス・トムソンの権威によっている。しかし、Lit & Phil のドルトンの実験室で発見されたノートの分析により[3]、倍数比例の法則が何故成り立つのかを考える過程で、一定の質量比率の原子の相互作用によって化学反応が起きているという考え方に到達した、すなわち、大気や他の気体の物理特性を研究する過程で純粋に物理的概念として原子説の考え方に至ったと断定された。この考え方は前述のドルトンの法則を提示した液体による気体の吸収に関する論文の最後の方に初めて書かれているが、論文の発表は1803年10月21日で、それが出版されたのは1805年のことである。ドルトンは次のように記している。
何故、水はあらゆる気体を同じ量だけ吸収しないのか? 私はこの疑問を当然考察し、自身で完全に納得したわけではないが、気体を構成する究極の粒子の数および質量に依存するのではないかとほぼ確信している。
原子
ドルトンは相対原子質量(原子量)の表を出版した。最初の表には、水素、酸素、窒素、炭素、硫黄、リンという6種類の元素が掲載されており、水素原子の質量を1としている。この論文では、どうやってそれらの値に到達したのかは説明されていない。しかし、実験室のノートには1803年9月6日付け[4]で、同時代の化学者らによる水、アンモニア、二酸化炭素などの分析からそれら元素の相対原子質量を求めたことがわかった。
気体が全て原子から成ると確信したドルトンは、次に原子の相対的大きさ(直径)を求めるという問題に直面した。そして組み合わせは常に可能な限り単純なものになると仮定し、化学反応が異なる質量の粒子の組み合わせで起きるという考え方に到達した。この点が古代ギリシアのデモクリトスやルクレティウスの原子論と異なる点である[要出典]
この考え方を物質全般に拡張することで倍数比例の法則が導かれ、実験によってそれが正しいことを確認した[5]。「酸素はある量の窒素またはその倍の量の窒素を化合するが、その中間の量の窒素とは化合しない」という倍数比例の法則の元になったと思われる記述が1802年11月に発表した論文にあるが、この論文が実際に出版されたのは1805年であり、その間に加筆された可能性も否定できない。
1808年の著作 New System of Chemical Philosophy には2原子、3原子、4原子の分子などが化合物を表す最も単純な形態として一覧で描かれている。
彼は化合物の構造が整数比率で表されると仮定した。従って、元素Xの原子1個と元素Yの原子1個が結びついて2元化合物となり、元素Xの原子1個と元素Yの原子2個(またはその逆)が結びついて3元化合物になるとした。New System of Chemical Philosophy に示された化合物の構造は、現代の観点から見て正しいものもあれば、間違っているものもある。
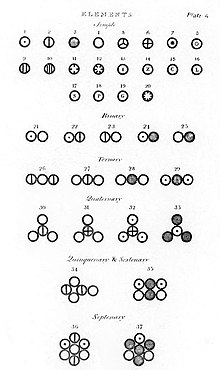
彼は元素記号も発表したが、それは黒く塗りつぶされた丸が炭素を表す、といったようなものであったため広まりはしなかったものの、歴史的な意義はあった。New System of Chemical Philosophy ではその記号を使って元素や化合物を表している。
原子論5つの原則
- ある元素の原子は、他の元素の原子とは異なる。異なる元素の原子は相対原子質量によって互いに区別できる。
- 同じ元素の原子は、同じ大きさ、質量、性質を持つ。
- 化合物は、異なる原子が一定の割合で結合してできる。
- 化学反応は、原子と原子の結合の仕方が変化するだけで、新たに原子が生成したり、消滅することはない。
- 元素は原子と呼ばれる小さな粒子でできている。
ドルトンは次のような「単純さ最大の法則」も提唱したが、独自に検証できなかったため論争を生んだ。
- 元素がある特定の比率でのみ結合するとき、それに反する証拠がない限り最も小さい整数個の原子が化合すると推定すべきである。
これは、自然の単純さへのドルトンの確信から生まれた単なる仮説だった。当時、化合物の分子を構成する原子が何個なのかを推論できる証拠は存在しなかった。しかし、相対原子質量を求めるには何らかの分子式を仮定する必要があり、このような法則は初期の理論には必須だった。ともかく「単純さ最大の法則」により、ドルトンは水の分子式が OH、アンモニアの分子式が NH だと推定し、それらは間違っていた。
ドルトンの原子説はその根幹が不確かだったが、その原則は生き残った。確かに、化学反応において原子がさらに小さな粒子に分裂したり、原子が生成したり破壊されたりしないという原則は、原子核融合や原子核分裂の存在と相容れないとも言えるが、そういった反応は原子核反応であって化学反応ではないとも言える。さらに原子には少しだけ質量の異なる同位体が存在するため、同じ元素の原子は同じ大きさ・質量・性質を持つという原則は正確ではない。それでもドルトンの生み出した原子説は極めて重要であり、アントワーヌ・ラヴォアジエの質量保存の法則以来の化学史上の重大な進歩だった。
- ^ Smith 1856, p. 279
- ^ George Hadley Encyclopedia Britannica. Accessed 2009-04-30.
- ^ Roscoe 1896
- ^ Roscoe 1896, p. 248
- ^ Roscoe 1896, pp. 50–51
- ^ "Dalton; John (1766 - 1844)". Record (英語). The Royal Society. 2011年12月11日閲覧。
- ^ Patterson 1970
- ^ Elliott, T. Lenton (1953). “John Dalton's Grave”. Journal of Chemical Education 30: 569. doi:10.1021/ed030p569.
- ^ Millington 1906, pp. 201–208
- ^ “Dalton Division”. 2021年2月18日閲覧。
- ^ “Dalton Transactions”. 2021年2月18日閲覧。
固有名詞の分類
| 化学者 |
ライナス・ポーリング ユストゥス・フォン・リービッヒ ジョン・ドルトン カール・ノイベルグ 杜祖健 |
| イギリスの物理学者 |
チャールズ・バーノン・ボーイズ ウイリアム・ウォラストン ジョン・ドルトン ゴードン・ドブソン ペーター・ヒルシュ |
| イギリスの化学者 |
ウイリアム・ウォラストン ウォルター・ハース ジョン・ドルトン ジェームズ・スミソン デレック・バートン |
| イングランドの化学者 |
ロバート・ボイル ジョゼフ・プリーストリー マイケル・ファラデー ハンフリー・デービー ジョン・ドルトン |
- ジョン・ドルトンのページへのリンク