
¿Qué es el carbono?
El carbono es un elemento químico no metálico cuyo símbolo químico es C. Se debe su nombre al carbón, vegetal o mineral, en donde sus átomos definen variadas estructuras. Forma una amplia gama de compuestos orgánicos e inorgánicos, y se presenta además en un considerable número de alótropos.
Se halla en todos los seres vivos. Todas sus biomoléculas deben su existencia a la estabilidad y fuerza de los enlaces C-C y su alta tendencia a concatenarse. Es el elemento de la vida, y con sus átomos se construyen sus cuerpos.
Los compuestos orgánicos con los que se construyen los biomateriales consisten prácticamente en esqueletos carbonados y heteroátomos. Estos pueden apreciarse a simple vista en la madera de los árboles, y también, cuando un rayo cae sobre ellos y los rostiza. El sólido negro inerte remanente también posee carbono, pero se trata de carbón vegetal.
Propiedades del carbono
Las propiedades físicas o químicas halladas en los sólidos, minerales o materiales carbonáceos están sujetas a muchas variables. Entre ellas están: la composición o grado de impurezas, las hibridaciones de los átomos de carbono, la diversidad de las estructuras y la morfología o tamaño de los poros.
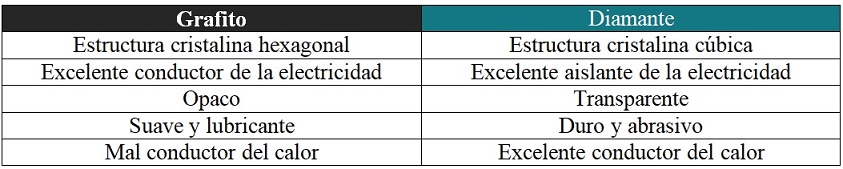
Cuando se describen las propiedades del carbono, la mayoría de los textos o fuentes bibliográficas se basan en el grafito y el diamante. Es porque son los alótropos más conocidos para este elemento y representan sólidos o materiales de alta pureza, es decir, prácticamente están hechos nada más que de átomos de carbono (aunque con distintas estructuras).
Las propiedades del carbón vegetal y del carbón mineral difieren en sus orígenes o composiciones, respectivamente. Por ejemplo, el lignito (pobre en carbono) como combustible gatea en comparación a la antracita (rica en carbono). Y qué decir de los otros alótropos: nanotubos, fulerenos, grafenos, grafinos, etc.
Sin embargo, químicamente tienen un punto en común: se oxidan con un exceso de oxígeno en CO₂:
C + O2 => CO₂
Ahora bien, la velocidad o temperatura que requieren para oxidarse son propias para cada uno de estos alótropos.
Grafito vs. diamante
Aquí se hará también un breve comentario respecto a las propiedades diferentes para estos dos alótropos:
Estructura y configuración electrónica del carbono
Hibridaciones
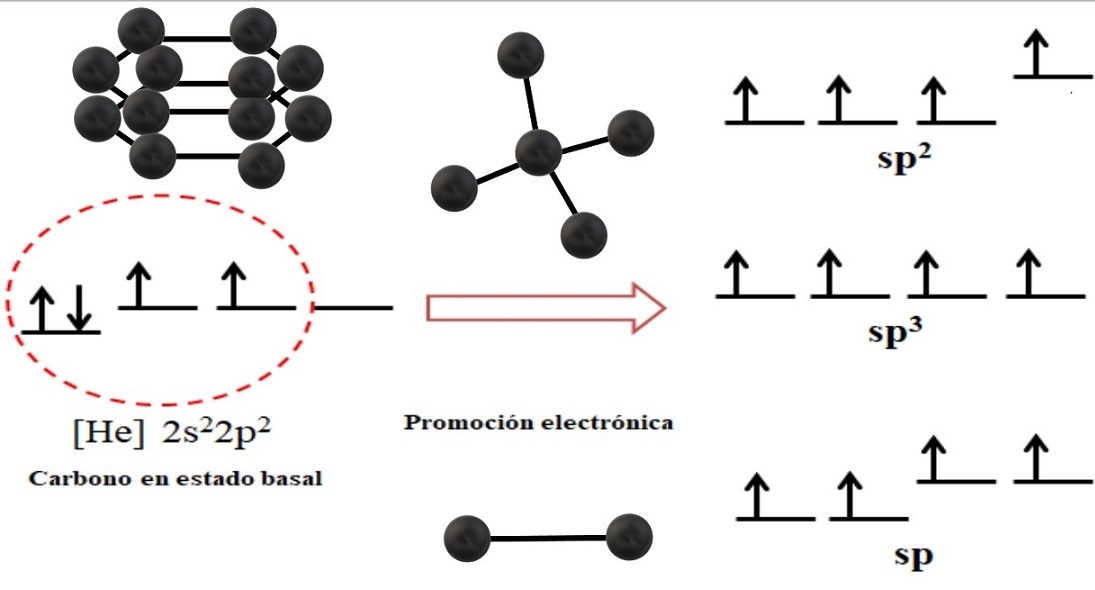
La configuración electrónica para el átomo de carbono es 1s22s22p2, también escrita como [He]2s22p2 (imagen superior). Esta representación corresponde a su estado basal: el átomo de carbono aislado y suspendido en un vacío tal que no puede interactuar con otros.
Se aprecia que uno de sus orbitales 2p carece de electrones, el cual acepta mediante la promoción electrónica un electrón del orbital 2s de menor energía, y así, el átomo adquiere la capacidad de formar hasta cuatro enlaces covalentes a través de sus cuatro orbitales híbridos sp3.
Nótese que los cuatro orbitales sp3 están degenerados en energía (alineados en el mismo nivel). Los orbitales p puros son más energéticos, razón por la que se sitúan por encima de los otros orbitales híbridos (a la derecha de la imagen).
Si hay tres orbitales híbridos, es porque resta un orbital p sin hibridizarse. Por lo tanto, se trata de tres orbitales sp2. Y cuando hay dos de estos orbitales híbridos, dos orbitales p están disponibles para formar dobles o triples enlaces, siendo la hibridación del carbono sp.
Tales aspectos electrónicos son imprescindibles para comprender por qué el carbono puede hallarse en infinidad de alótropos.
Números de oxidación
Antes de proseguir con las estructuras no está de más mencionar que, dada la configuración electrónica de valencia 2s22p2, el carbono puede tener los siguientes números de oxidación: +4, +2, 0, -2 y -4.
Estos números corresponden a la suposición de que exista un enlace iónico tal que forme los iones con las cargas respectivas, es decir, C4+, C2+, C0 (neutro), C2- y C4-.
Para que el carbono tenga un número de oxidación positivo debe perder electrones, y para hacerlo, necesariamente tiene que estar enlazado a átomos muy electronegativos (como el oxígeno).
Mientras, para que el carbono tenga un número de oxidación negativo, debe ganar electrones enlazándose a átomos metálicos o menos electronegativos que él (como el hidrógeno).
El primer número de oxidación, +4, significa que el carbono ha perdido todos los electrones de valencia. Se quedan vacíos los orbitales 2s y 2p. Si el orbital 2p pierde sus dos electrones, el carbono tendrá número de oxidación de +2. Si gana dos electrones, tendrá -2, y si gana dos electrones más completando su octeto de valencia, -4.
Ejemplos
Por ejemplo, para el CO₂ el número de oxidación del carbono es +4 (porque el oxígeno es más electronegativo), mientras que para el CH4, es de -4 (porque el hidrógeno es menos electronegativo).
Para el CH3OH, el número de oxidación del carbono es -2 (+1 para los H y -2 para el O), mientras que para el HCOOH, es de +2 (compruebe que la suma dé 0).
Otros estados de oxidación, como el -3 y +3, también son probables, en especial cuando se trata de moléculas orgánicas. Por ejemplo, en los grupos metilos, -CH3.
Geometrías moleculares
En la imagen superior no solo se mostraron la hibridación de los orbitales para el átomo de carbono, sino además las geometrías moleculares resultantes cuando se enlazan varios átomos (esferas negras) a uno central. Este átomo central, para disponer en el espacio un entorno geométrico determinado, debe poseer la respectiva hibridación química que se lo permita.
Por ejemplo, para el tetraedro, el carbono central tiene hibridación sp3, porque tal es el arreglo más estable para los cuatro orbitales híbridos sp3. En el caso de los carbonos sp2, pueden formar dobles enlaces y disponer un entorno plano trigonal, y así, estos triángulos definen un hexágono perfecto. Y para una hibridación sp, los carbonos adoptan una geometría lineal.
Así, las geometrías observadas en las estructuras de todos los alótropos se rigen simplemente en tetraedros (sp3), hexágonos o pentágonos (sp2), y líneas (sp).
Los tetraedros definen una estructura 3D, mientras que los hexágonos, pentágonos y líneas, estructuras 3D o 2D. Estas últimas vienen a ser los planos o láminas similares a las paredes de los panales de abeja:

Y si plegamos dicha pared hexagonal (pentagonal o mixta), obtendremos un tubo (nanotubos) o un balón (fulerenos), u otra figura. Las interacciones entre estas figuras dan lugar a diferentes morfologías.
Sólidos amorfos o cristalinos
Dejando a un lado las geometrías, hibridaciones o morfologías de las estructuras posibles del carbono, sus sólidos pueden clasificarse globalmente en dos tipos: amorfos o cristalinos. Y entre estas dos clasificaciones se reparten sus alótropos.
El carbono amorfo es el que presenta una mezcla arbitraria de tetraedros, hexágonos o líneas, incapaz de establecer un patrón estructural, como el caso de la hulla, el carbón vegetal o activado, coque, hollín, etc.
El carbono cristalino consta de patrones estructurales conformados por cualquiera de las geometrías planteadas, por ejemplo, el diamante (red tridimensional de tetraedros) y el grafito (láminas hexagonales apiladas).
¿Dónde se encuentra el carbono?
Además de ser el elemento químico componente común en todas las formas de vida, el carbono en la naturaleza está presente en tres formas cristalinas: diamante, grafito y fulereno.
También existen varias formas minerales amorfas de carbón (antracita, lignito, hulla, turba), formas líquidas (variedades de petróleos) y gaseosas (gas natural).
Usos del carbono
Nuevamente, al igual que las propiedades y estructura, los usos o aplicaciones van acorde con los alótropos o formas mineralógicas del carbono. Sin embargo, existen ciertas generalidades que pueden mencionarse, además de algunos puntos altamente conocidos.
- Reducción de metales. El carbono se ha utilizado desde hace mucho tiempo como agente reductor de minerales en la obtención de los metales puros, como hierro, silicio y fósforo, entre otros.
- Vida. Es la piedra angular de la vida, y la química orgánica y la bioquímica son los estudios de este reflejo.
- Combustible. También ha sido un combustible fósil que permitió que las primeras máquinas pudiesen funcionar. Del mismo modo, de él se obtuvo el gas de carbono para los viejos sistemas de iluminación. El carbón fue sinónimo de luz, calor y energía.
- Aceros. Mezclado como aditivo con el hierro en distintas proporciones, permitió la invención y perfeccionamiento de los aceros.
- Arte. El grafito se utilizó en el arte.
Riesgos y precauciones del carbono
El carbono y sus sólidos no representan ningún riesgo para la salud (como el carbón para las parrillas).
El coque, por otro lado, puede representar un riesgo si su contenido de azufre es alto. Al combustionar liberará gases sulfurados que, además de ser tóxicos, contribuyen a la lluvia ácida. Y aunque el CO₂ en pequeñas cantidades no puede asfixiarnos, sí ejerce un enorme impacto en el medio ambiente como gas invernadero.
Desde esta perspectiva, el carbono es un peligro “a largo plazo”, ya que su combustión altera el clima de nuestro planeta.
Y en un sentido más físico, los sólidos o materiales carbonáceos si se encuentran pulverizados son fácilmente transportados por las corrientes de aire, y en consecuencia, se introducen a los pulmones, lo cual puede dañarlos irremediablemente.
Referencias
- Morrison, R. T. y Boyd, R, N. Química Orgánica. 5ta Edición. Editorial Addison-Wesley Interamericana.
- Graham Solomons, T.W., Craig B. Fryhle. Organic Chemistry. Amines. (10th edition). Wiley Plus.