REVISIÓN DEL TEMA
La resonancia magnética utiliza las características de relajación de los protones,
basándose en los parámetros de relajación T1,
T2 y T2*,
para caracterizar el tejido miocárdico.
Cambios en el tiempo de relajación del tejido miocárdico en las secuencias T1 (con o sin contraste intravenoso),
T2 y T2* pueden reflejar la presencia de enfermedad miocárdica.
La elección adecuada de dichas secuencias y el conocimiento del comportamiento de los tejidos en cada una de ellas,
permiten realizar un estudio exhaustivo de la patología cardíaca.
SECUENCIAS SANGRE NEGRA
Este tipo de secuencias se basan en la secuencia clásica eco del espín (ES),
en la que se incluye una consecución de dos pulsos de inversión recuperación (DIR) para anular la señal de la sangre con flujo rápido.
Esta anulación de la señal de la sangre produce un excelente contraste de la pared miocárdica.
Se usan secuencias de lectura rápida (fast o turbo ES),
para acortar el tiempo de adquisición (3).
-T1 ECO DEL ESPÍN (T1 ES)
Habitualmente se utiliza para el estudio morfológico del corazón y los grandes vasos.
En cuanto a la caracterización tisular miocárdica,
contribuye en el análisis de las masas cardíacas y es especialmente útil para determinar la presencia de tejido con T1 corto,
es decir,
hiperintenso T1 (grasa,
melanina,
hemorragia,
líquidos de contenido exudativo).
Para diferenciar la presencia de grasa intramiocárdica frente a otros tejidos con T1 corto,
se recomienda el uso de secuencias T1 ES,
sin y con un pulso selectivo de saturación grasa (T1 ES SG).
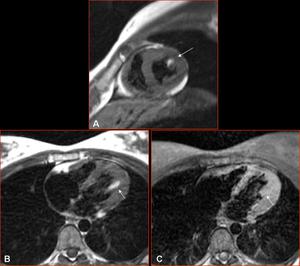
Fig. 1: A)T1 ES eje corto, B) T1 ES axial, C) T1 ES SG axial. En ecocardiografía, sospecha de nódulo en músculo papilar anterior. En las secuencias ES T1 se objetiva un nódulo hiperintenso T1, isointenso con respecto a la grasa subcutánea, cuya señal se suprime en la secuencia T1 ES SG (flecha). El hallazgo es compatible con lipoma intramuscular.
-T2 ECO DEL ESPIN (T2 ES)
Se utiliza principalmente para la detección de edema miocárdico,
como ocurre en la enfermedad miocárdica aguda (isquémica o inflamatoria),
porque el tiempo de relajación T2 del agua es largo y por lo tanto brillará (4).
El flujo intracavitario y la grasa pericárdica puede producir alta señal y confundirse con edema.
Para evitarlo,
las secuencias T2 para estudio miocárdico incluyen un triple pulso de inversión recuperación (TIR),
para suprimir la señal del flujo y de la grasa.
Habitualmente se realiza una valoración visual de las imágenes.
No obstante,
se puede realizar también una valoración semicuantitativa,
tomando como referencia las áreas de miocardio no edematosas o la musculatura estriada.
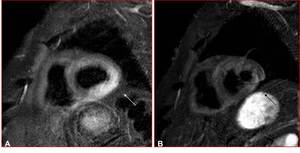
Fig. 2: A y B) STIR-T2 eje corto. Ingreso por episodio de SCASEST. Infarto agudo miocárdico inferolateral. A) Hiperseñal miocárdica inferolateral compatible con edema (flecha blanca). B) Control realizado a las dos semanas. Marcada disminución de la extensión y la intensidad de señal del edema (flecha negra).
SECUENCIA SANGRE BLANCA
PRECESIÓN LIBRE EN ESTADO ESTACIONARIO (SSFP)
Hoy en día es la secuencia sangre blanca más utilizada para el análisis cardíaco.
Se conoce de forma genérica mediante las siglas SSFP,
correspondientes a sus siglas en inglés (steady-state free precession).
Es una secuencia eco de gradiente,
habitualmente obtenida en modo cine,
con un excelente contraste entre el flujo sanguíneo (hiperintenso) y el miocardio a lo largo del ciclo cardíaco.
Por ello,
su uso está dirigido a la valoración de la morfología y la función miocárdica.
La señal está influenciada tanto por la relajación T1 como T2.
Normalmente,
no se emplea para la valoración de los tejidos aunque,
en ocasiones,
el comportamiento de los mismos en estas secuencias puede corroborar el diagnóstico (5).
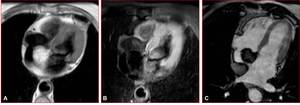
Fig. 3: A) T1 ES y B) T1 ES SG axial. C) SSFP 4 cámaras. A) Importante engrosamiento septal interauricular, hiperointenso T1, isointenso con respecto a la grasa subcutánea. B) La señal se suprime de forma completa en la imagen T1 ES SG. C) Respeta la ventana oval. La ocupación por tejido graso (hipertrofia lipomatosa, lipoma), típicamente presenta un anillo periférico de baja señal, debido a la fase opuesta en la interfase grasa-líquido. Los hallazgos son compatibles con hipertrofia lipomatosa del septo interauricular.
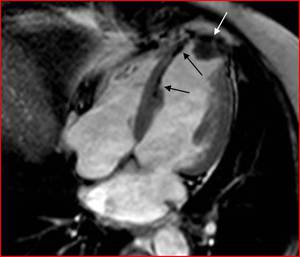
Fig. 4: Secuencia SSFP 4 cámaras. Adelgazamiento miocárdico septal medioapical y ápex de morfología ligeramente aneurismática, secundario a infarto crónico. Línea subendocárdica de baja señal en los segmentos afectados (flechas negras), compatible con metaplasia lipomatosa, hallazgo común en la cicatriz del infarto. El artefacto de desplazamiento químico en el límite grasa-agua, en el seno de la cicatriz, permiten su detección en RM. Defecto hipointenso intracavitario apical compatible con trombo (flecha blanca).
SECUENCIAS CON CONTRASTE INTRAVENOSO (GADOLINIO)
Como contraste intravenoso se utilizan los quelatos de gadolinio.
Son contrastes paramagnéticos,
por lo que acortan el tiempo de relajación T1 del tejido captante.
Se requieren secuencias ponderadas en T1 para valorar este efecto.
Los quelatos de gadolinio son contrastes extracelulares que difunden rápidamente desde los capilares al espacio intersticial,
pero no al espacio intracelular.
PERFUSIÓN MIOCÁRDICA (6)
La cardio-RM con contraste ha demostrado ser un método válido en el estudio de la perfusión miocárdica.
Habitualmente el estudio se realiza en reposo y tras estrés farmacológico.
Permite poner de manifiesto defectos de perfusión miocárdicos.
Utiliza la ”técnica de perfusión de primer paso”,
es decir,
secuencias eco de gradiente ultrarrápidas,
de alta potenciación T1,
con alta resolución temporal,
adecuada resolución y cobertura espacial y máxima relación señal/ruido que permitan obtener imágenes en el primer tránsito del bolo de contraste por el corazón para analizar la perfusión miocárdica.
Generalmente,
la hipoperfusión traduce isquemia por estenosis coronaria significativa. La arteria coronaria estenosada reacciona de forma compensatoria con una dilatación máxima.
La administración del fármaco provoca un efecto vasodilatador en el resto del territorio coronario,
que generará una reducción de la perfusión en el territorio irrigado por la arteria estenótica,
donde se generará isquemia (fenómeno de “Robo coronario”).
Las zonas hipoperfundidas se verán en los primeros minutos como áreas de intensidad de señal disminuida a diferencia del miocardio normoperfundido que se verá hiperintenso.
En la práctica,
el análisis de la perfusión se realiza habitualmente de forma cualitativa,
mediante la detección visual subjetiva de los defectos de perfusión miocárdica,
aunque también se puede realizar de forma semicuantitativa o cuantitativa.
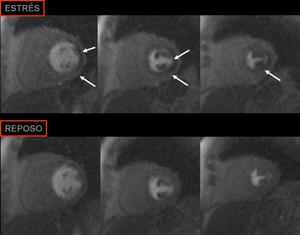
Fig. 5: Perfusión miocárdica, eje corto basal, medio y apical. Defecto de perfusión subendocárdico lateral (flechas blancas) inducido mediante estrés farmacológico en paciente con oclusión proximal de arteria circunfleja.
References: Resonancia Magnética Osatek Galdakao (Vizcaya)/ES
REALCE MIOCÁRDICO
-Realce tardío
Tanto el tejido sano como el miocardio dañado captan contraste.
Sin embargo,
en el miocardio sano se produce un lavado rápido del contraste,
mientras que en el tejido dañado el lavado es más lento y el contraste permanece más tiempo.
Para evidenciar este fenómeno,
se emplean secuencias eco de gradiente ponderadas en T1 a las que se le aplica un pulso de inversión-recuperación que anula la señal del miocardio sano; de este modo,
se obtiene el máximo contraste entre el miocardio sano (hipointenso) y el miocardio lesionado (hiperintenso).
La ventana de tiempo recomendada para la obtención de las imágenes que nos permitan distinguir el miocardio sano lavado,
del patólogico que todavía retiene contraste,
es entre los 10 y 25 minutos después de la inyección del gadolinio.
Un aspecto importante de esta secuencia es que el tiempo de inversión para la supresión de la señal del miocardio sano se ha de elegir en cada paciente.
Habitualmente se evalúa de forma visual,
aunque también se puede cuantificar las áreas de captación (por ejemplo,
en el infarto).
Constituye una de las mayores aportaciones dela RM puesto que el patrón de captación y su distribución aportan una información importante en el diagnóstico diferencial de las miocardiopatías (7).
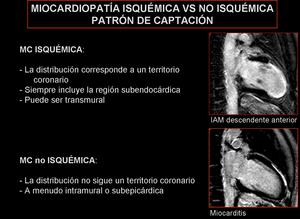
Fig. 6
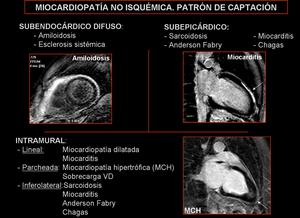
Fig. 7
-Realce precoz
En ocasiones,
se recomienda la adquisición de las imágenes en un periodo de tiempo precoz (1-4 minutos tras la administración de contraste):
-Miocarditis aguda: valora el grado de hiperemia y el aumento de la permeabilidad capilar,
debida a la vasodilatación del tejido inflamado. Constituye uno de los criterios diagnósticos de miocarditis por RM.
Se puede valorar visualmente o cuantitativamente (8).
-Infarto agudo de miocardio:
-Fenómeno de “no-reflow”: Valorable también mediante la técnica de perfusión.
Describe una situación de persistencia de hipoperfusión miocárdica en áreas que han sufrido un infarto, aun después de abrir la arteria epicárdica,
debido a un fenómeno de obstrucción microvascular coronaria.
Se presentan como áreas subendocárdicas hipointensas en el seno de la captación del infarto reperfundido.
- Trombo intracavitario: mejora su detección,
gracias a un mayor contraste entre el trombo y la sangre.
Se visualizan como defectos hipointensos intracavitarios.
El trombo organizado puede tener cierto grado de neovascularización,
por lo que se objetiva mejor en la adquisición precoz,
ya que puede captar en el realce tardío.
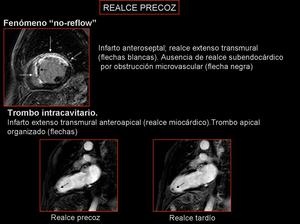
Fig. 8
DIAGNÓSTICOS DIFERENCIALES FRECUENTES
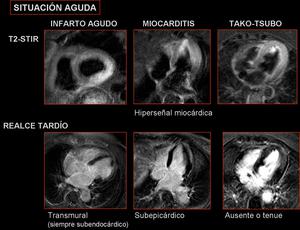
Fig. 9
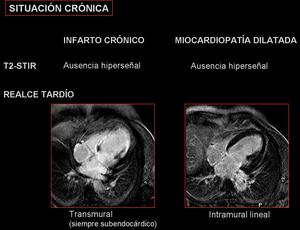
Fig. 10
NUEVOS AVANCES: MAPAS PARAMÉTRICOS
El reciente y rápido desarrollo tecnológico en RM,
ha hecho posible la obtención de mapas paramétricos de la perfusión o de las propiedades de relajación magnética (tiempo de relajación T1,
T2,
T2*),
que permiten cuantificar los daños producidos a nivel tisular.
Para generar un mapa paramétrico,
se requieren secuencias muy rápidas,
mediante las que se obtienen múltiples imágenes de la misma región miocárdica,
con distintas sensibilidades para el parámetro de interés.
Las intensidades de señal de estas imágenes se ajustan a un modelo,
el cual estima los valores a partir de los cuales se construye el mapa paramétrico.
El mapa paramétrico obtenido corresponde a una imagen a partir de la cual podremos obtener las medidas de perfusión o de tiempo de relajación.
Mediante la presentación en color se puede hacer un análisis visual (9).
MAPA PARAMÉTRICO T2*(10)
Entre las técnicas de cuantificación para la caracterización tisular mediante RM,
es la más consolidada en la práctica clínica.
Ha supuesto una revolución en la detección y monitorización de las miocardiopatías que puedan cursar con sobrecarga de hierro miocárdico.
El depósito de hierro provoca un aumento de las inhomogeneidades de campo,
lo que a su vez da lugar a un mayor acortamiento del tiempo de relajación T2*.
Existe una relación inversa entre el valor T2* y la concentración de hierro miocárdica,
lo que permite utilizar este parámetro para identificar y cuantificar la sobrecarga miocárdica.
El valor T2* es altamente predictivo del riesgo de miocardiopatía debida a sobrecarga férrica.
Los pacientes con valores T2*miocárdico (T2*M) mayores que 20ms (no se detecta hierro cardíaco) no desarrollan disfunción cardíaca,
mientras que pacientes con T2*M menores que 10ms se encuentran en alto riesgo de descompensación cardíaca.
Esta técnica ha demostrado ser reproductible y transferible a la rutina clínica.
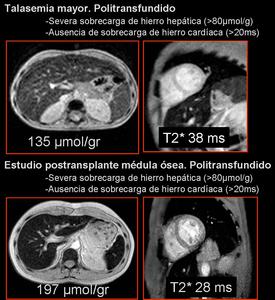
Fig. 11
MAPA PARAMÉTRICO T1 (11)
Se realiza sin y con contraste intravenoso.
Permite obtener medidas cuantitativas del T1 miocárdico y de la sangre,
claves para cuantificar el daño miocárdico tanto regional como difuso.
-Medición T1 sin contraste (T1 nativo): refleja la enfermedad miocárdica que envuelve al miocito y al espacio intersticial.
El tiempo de relajación T1 normal para una RM de 1,5T,
se estima que se encuentra en el rango de 900-1100ms,
con algunas variaciones dependiendo de la técnica.
Sin necesidad de contraste,
permite determinar la presencia de enfermedad miocárdica. Puede aumentar el T1 en situaciones como el infarto agudo,
miocarditis,
fibrosis focal o difusa o amiloidosis cardíaca.
Se ha descrito disminución del T1 en la enfermedad de Anderson-Fabry y en la siderosis.
Iincluso se sugiere que mediante esta técnica se pueda detectar afectación cardíaca no sospechada o en estadio preclínico.
- Cálculo de la fracción de volumen extracelular: refleja variaciones en el espacio extracelular (EEC) miocárdico en base a las variaciones de T1 debidas a la presencia de contraste extracelular.
Esta información se obtiene calculando las diferencias en T1,
tanto de la sangre como del músculo cardiaco,
antes y después de la inyección del contraste,
asumiendo que estas diferencias se deben al depósito del contraste en el EEC.
En ausencia de edema o depósito de amiloide,
el colágeno es el principal responsable de la expansión del EEC,
que a su vez da lugar a alteraciones eléctricas,
mecánicas y vasomotoras,
que aumentan la vulnerabilidad miocárdica. Algunos datos indican que la medición del volumen extracelular tiene un valor pronóstico tan importante como la fracción de eyección ventricular izquierda,
lo que a su vez destaca la importancia del intersticio en la enfermedad miocárdica.
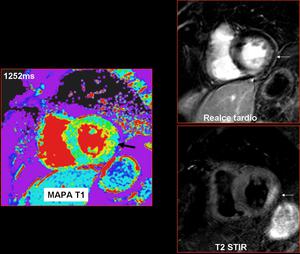
Fig. 12: Antecedentes personales: Cardiopatía isquémica intervenida. Ingreso por dolor torácico agudo. Troponinas 1540. A) Edema y B) realce tardío miocárdico lateral (flechas blancas), compatible con infarto agudo de miocardio. C) Mapa T1 nativo: El valor T1 sin contraste (1252ms) se encuentra aumentado (flecha gruesa).
MAPA PARAMÉTRICO T2 (12)
Cuantifica el tiempo de relajación T2 del miocardio,
prolongado en regiones miocárdicas edematosas o inflamadas (infarto agudo,
miocarditis,
enfermedad de Tako-Tsubo,
rechazo al transplante cardíaco).
Los valores T2 del miocardio normal corresponden a 52-55ms.
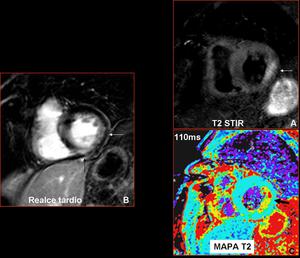
Fig. 13: Mismo paciente que la figura 12. C) Mapa paramétrico T2: Aumento del valor T2 (110ms) (flecha gruesa). B) Infarto crónico inferior (flecha negra)
CUANTIFICACIÓN DE LA PERFUSIÓN MIOCÁRDICA
Permite determinar de forma más exacta la extensión de la isquemia miocárdica en la enfermedad coronaria y evaluar la enfermedad microvascular.
Existen diversos modelos de medida de perfusión para la RM y múltiples estudios que demuestran la capacidad de la RM para la cuantificación de la perfusión miocárdica.
Las secuencias basadas en mapas paramétricos se encuentran en la actualidad en desarrollo.














