Abkömmlinge des Contergan-Wirkstoffs Thalidomid eignen sich womöglich als Tumor-Medikamente. In diese Richtung deutet eine Studie der Goethe-Universität Frankfurt. Thalidomid wurde in den 1950er-Jahren als Schlafmittel verkauft. Es erlangte später traurige Berühmtheit, da es bei heranreifenden Kindern im Mutterleib schwere Fehlbildungen hervorruft. Inzwischen ist bekannt, dass das Molekül Proteine in der Zelle für den Abbau markiert. In der aktuellen Arbeit stellten die Forschenden Derivate des Wirkstoffs her. Sie konnten zeigen, dass unter ihrem Einfluss Proteine abgebaut werden, die das Überleben von Krebszellen sichern.
Kaum ein Wirkstoff hat eine so bewegte Geschichte hinter sich wie Thalidomid. Das Molekül ist der zentrale Inhaltsstoff von Contergan, das in den 1950er-Jahren in vielen Ländern als Beruhigungs- und Schlafmittel zugelassen wurde. Doch bald stellte sich heraus, dass Schwangere, die Contergan genommen hatten, oft Kinder mit schweren Fehlbildungen zur Welt brachten.
Und dennoch setzt die Medizin seit einigen Jahrzehnten wieder große Hoffnung in den Wirkstoff. Denn in Studien zeigte sich unter anderem, dass er das Wachstum von Blutgefäßen unterbindet und sich damit möglicherweise eignet, um Tumoren von ihrer Nährstoffversorgung abzuschneiden. Später erwies er sich zudem als sehr effektiv für die Behandlung von Multiplen Myelomen, bösartigen Tumoren im Knochenmark.
„Wir wissen inzwischen, dass Thalidomid ein sogenannter molekularer Klebstoff ist“, erklärt Dr. Xinlai Cheng vom Institut für Pharmazeutische Chemie der Universität Frankfurt. „Das heißt, der Wirkstoff hat die Fähigkeit, zwei Proteine zu greifen und so in Nähe zueinander zu bringen.“ Interessant ist das vor allem deshalb, weil es sich bei einem dieser Proteine um eine Art Etikettiermaschine handelt: Es heftet dem anderen Protein ein Label an, auf dem in großen Lettern „muss entsorgt werden“ steht.
Dieses Label wird von der zellulären Müllabfuhr erkannt: Sie ergreift das markierte Eiweißmolekül und schreddert es. „Genau dieser Mechanismus ist es, der die verschiedenen Wirkungen von Thalidomid erklärt“, sagt Cheng. „Je nachdem, welches Protein markiert wird, kann das bei der Embryonalentwicklung zu Fehlbildungen führen oder eben einen Tumor abtöten.“
Für die Medizin eröffnet dieser Mechanismus große Möglichkeiten. Denn Krebszellen sind auf bestimmte Proteine angewiesen, um zu überleben. Könnte man diese gezielt schreddern, ließen sich die Krankheiten damit vielleicht heilen. Das Problem ist nur: Molekularer Klebstoff wirkt ziemlich spezifisch. Einer seiner Bindungspartner ist stets die zelluläre Etikettiermaschine, fachsprachlich: eine E3-Ligase namens CRBN. Als anderer Partner kommen nur sehr wenige der vielen Tausend Proteine im Körper in Frage – welche genau, ist von Klebstoff zu Klebstoff verschieden.
„Wir haben daher eine Reihe von Thalidomid-Derivaten hergestellt“, sagt Cheng. „Dann haben wir überprüft, ob sie Klebstoff-Eigenschaften haben und, falls ja, gegen welche Proteine sie wirken.“ Dazu haben die Forschenden ihre Derivate zu allen Proteinen einer Kulturzell-Linie gegeben. Danach haben sie überprüft, welche dieser Proteine unter Anwesenheit von CRBN abgebaut wurden.
„Wir sind dabei auf drei Derivate gestoßen, die ein sehr wichtiges Zellprotein für den Abbau markieren können, das BCL-2“, erklärt Cheng. „BCL-2 verhindert, dass das Selbstmord-Programm von Zellen aktiviert wird. Wenn es fehlt, gehen die Zellen daher zugrunde.“ BCL-2 ist daher schon seit einiger Zeit im Fokus der Krebsforschung. Es gibt sogar bereits einen Leukämie-Wirkstoff namens Venetoclax, der die BCL-2Wirksamkeit vermindert und entartete Zellen so in den Selbstmord treibt.
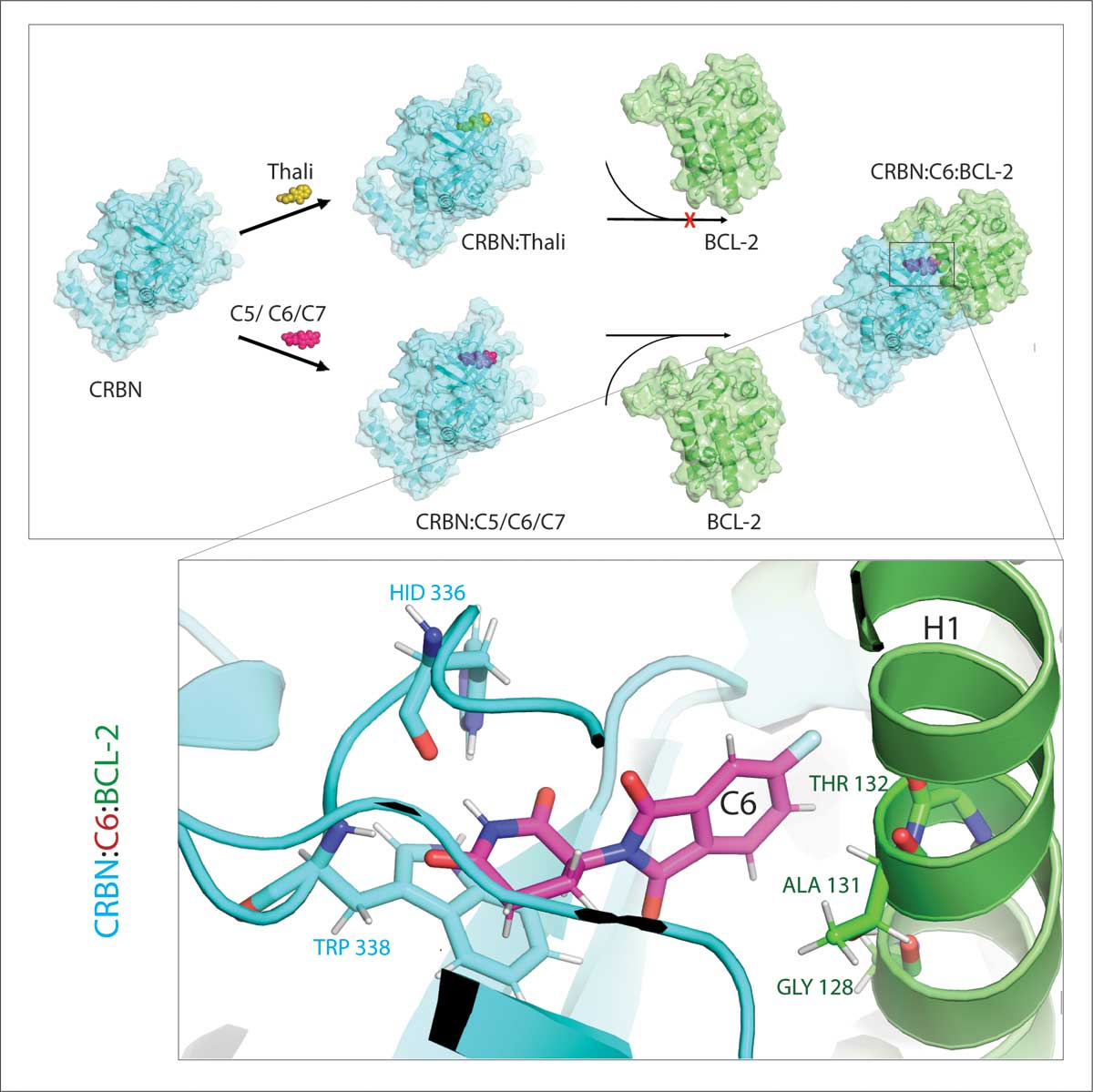
„In vielen Krebszellen ist BCL-2 aber mutiert, so dass Venetoclax das Protein nicht mehr hemmt“, sagt Cheng. „Wir konnten zeigen, dass unsere Derivate auch diese mutierte Form für den Abbau markieren. Unsere Partnerinnen und Partner vom Max-Planck-Institut für Biophysik haben die Interaktion der Thalidomid-Abkömmlinge mit BCL-2 zudem am Computer simuliert. Dabei zeigte sich, dass die Derivate an ganz andere Stellen binden als das Venetoclax – ein Ergebnis, das wir später auch noch experimentell bestätigen konnten.“
Die Forschenden testeten ihre Substanzen zudem in Taufliegen mit Tumorzellen. Die behandelten Fliegen überlebten dadurch deutlich häufiger. Allerdings handele es sich bei diesen Ergebnissen noch um Grundlagenforschung, warnt Cheng vor zu großen Erwartungen: „Sie zeigen zwar, dass veränderte Thalidomid-Moleküle ein großes therapeutisches Potenzial haben. Ob die Wirkstoffe sich irgendwann tatsächlich in der Praxis bewähren, lässt sich damit aber noch nicht sagen.“
Die Arbeit wurde vom DFG, Frankfurt Cancer Institute, und dem PROXIDRUGS-Projekt unterstützt.
Publikation: Jianhui Wang, Marcel Heinz, Kang Han, Varun J. Shah, Sebastian Hasselbeck, Martin P. Schwalm, Rajeshwari Rathore, Gerhard Hummer, Jun Zhou, Ivan Dikic, Xinlai Cheng: Thalidomide derivatives degrade BCL-2 by reprogramming the binding surface of CRBN; Cell Reports Physical Science (2024) https://doi.org/10.1016/j.xcrp.2024.101960













